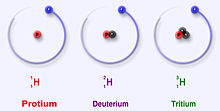
Vodík má tri hlavné izotopy: protórium (1H), deutérium (2H) a trícium (3H). Tieto izotopy vznikajú prirodzene v prírode. Protórium a deutérium sú stabilné. Trícium je rádioaktívne a má polčas rozpadu približne 12 rokov. Vedci vytvorili štyri ďalšie izotopy vodíka (4H to 7H), ale tieto izotopy sú veľmi nestabilné a v prírode sa nevyskytujú.
Hlavné izotopy vodíka sú jedinečné, pretože sú to jediné izotopy, ktoré majú svoje meno. Tieto názvy sa používajú dodnes. Deutérium a trícium niekedy dostávajú vlastné symboly D a T. Medzinárodná únia pre čistú a aplikovanú chémiu však tieto názvy nemá veľmi rada, aj keď sa často používajú. Existujú aj ďalšie izotopy, ktoré mali svoje vlastné názvy, keď vedci skúmali rádioaktivitu. Ich názvy sa však dnes už nepoužívajú.
Zloženie a základné vlastnosti
Protórium (1H) je najbežnejší izotop vodíka: jeho jadro tvorí jediný protón a žiadny neutrón. Protórium predstavuje približne 99,985 % všetkých atómov vodíka v prírode.
Deutérium (2H alebo D) má v jadre jeden protón a jeden neutrón. Je stabilné a v prírode sa vyskytuje v malom množstve — približne 0,0156 % (asi 156 častíc na milión) atómov vodíka. Chemické a fyzikálne vlastnosti látok obsahujúcich deutérium sa mierne líšia od bežných: napríklad ťažká voda (D2O) je hustejšia a má vyššie teploty topenia a varu než obyčajná voda.
Trícium (3H alebo T) má jedno protonové a dva neutrónové komponenty v jadre. Je rádioaktívne, rozpadá sa beta rozpadom na 3He; jeho polčas rozpadu je približne 12,3 rokov (zvyčajne sa udáva približne 12 rokov). Trícium sa v prírode vyskytuje len v stopovom množstve, ale vytvára sa aj umelo v jadrových zariadeniach.
Výskyt a pôvod
- Protórium a deutérium vznikli už počas veľkého tresku a následnej nukleosyntézy; relatívne množstvo deutéria je dôležité pre kozmológiu (slúži ako test modelov primordiálnej nukleosyntézy).
- Trícium vzniká prirodzene interakciou kozmického žiarenia s atmosférou, ale výraznejšie množstvá sa tvoria pri jadrových reakciách a v jadrových reaktoroch alebo pri testoch jadrových zbraní (historicky to výrazne zvýšilo hladiny trícia v atmosfére).
- Ďalšie izotopy vodíka (4H až 7H) boli zhotovené v laboratóriu pri experimentoch s urýchľovačmi častíc; sú však extrémne nestabilné a rozpadnú sa okamžite po vytvorení, preto v prírode prakticky neexistujú.
Použitie a význam
- Deutérium (a zlúčeniny bohaté na deutérium) sa využíva v jadrovej technike — napríklad ťažká voda D2O sa používa ako moderátor v niektorých typoch reaktorov. Deutérium je tiež dôležité v spektroskopii (deutériované rozpúšťadlá v NMR), vo výskume izotopických účinkov a ako stopovací izotop v environmentálnych štúdiách.
- Trícium sa používa ako stopovací rádioizotop v hydrológii a environmentálnych výskumoch, v osvetľovacích zariadeniach (luminiscenčné zdroje bez externého napájania), a je predmetom výskumu pri termonukleárnej syntéze (fúzia D–T sľubuje vysokú energetickú návratnosť).
- Izotopické zloženie vodíka v prírode (pomery D/H a T/H) sa využíva v paleoklimatológii, štúdiu kolobehu vody a v geochemických analýzach.
Meriacie metódy a izotopické účinky
Pomery izotopov sa merajú hmotnostnou spektrometriou, infračervenou spektroskopiou, NMR a ďalšími analytickými metódami. Prítomnosť ťažkého izotopu mení rýchlosti chemických reakcií a fyzikálne parametre — tomu sa hovorí izotopický efekt a je to dôležité napr. pri farmaceutickom vývoji či pri štúdiu reakčných mechanizmov.
Bezpečnosť a rádioaktivita
Trícium je slabý beta žiarič s nízkou energiou, takže jeho beta častice nepreniknú kožou. Najnebezpečnejší je pri vnútornom vstupe do organizmu (vdychovanie, požívanie alebo absorpcia cez rany), preto sa s ním v priemysle a výskume zaobchádza podľa prísnych pravidiel. Emisie trícia do životného prostredia sú regulované, pretože sa ľahko viaže na vodu a biologické systémy.
Krátky prehľad vzácnych izotopov
Izotopy 4H až 7H boli pozorované v experimentoch na urýchľovačoch. Tieto jadrá sú veľmi bohaté na neutrony vzhľadom k počtu protónov a sú extrémne nestabilné — štúdium ich vlastností pomáha pochopiť jadrové sily v extrémnych pomeroch a hranice viazania nukleónov.
Zhrnutie
Vodík má tri hlavné izotopy: protórium (najbežnejší, bez neutrónu), deutérium (stabilný, s jedným neutrónom) a trícium (rádioaktívny, s dvoma neutrónmi). Deutérium a trícium majú dôležitú úlohu v priemysle, vede a vo výskume (ťažká voda, stopovacie štúdie, fúzia). Ďalšie izotopy existujú len v laboratórnych podmienkach a sú výrazne nestabilné.