Atómy chemického prvku môžu existovať v rôznych formách nazývaných izotopy. Izotopy majú rovnaký počet protónov (a elektrónov), ale rôzny počet neutrónov, v dôsledku čoho sa líšia svojou hmotnosťou. Hmotnosť atómu vyjadruje, koľko látky alebo hmoty daný atóm predstavuje; rôzne izotopy toho istého prvku teda majú rovnaké chemické postavenie, ale rôznu nukleónovú (nukleón = protón alebo neutrón) hmotnosť.
Atómové číslo a hmotnostné číslo
Rôzne izotopy toho istého prvku majú rovnaké atómové číslo, teda rovnaký počet protónov, preto zaberajú v periodickej tabuľke prvkov to isté miesto. Rozlišujú sa podľa hmotnostného čísla (označuje súčet protónov a neutrónov). Počet neutrónov možno zistiť odčítaním atómového čísla od hmotnostného čísla.
Označenie izotopov
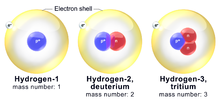
Bežné označenie izotopu je napríklad nazov-prvku-∕-hmotnostné číslo (napr. uhlík‑12, uhlík‑14) alebo vo forme AX, kde A je hmotnostné číslo a X symbol prvku. Pre vodík sa často uvádzajú špecifické názvy: protónium (1H), deutérium (2H), a tritium (3H), pričom deutérium a tritium sú izotopy vodíka s jedným, resp. dvoma neutrónmi.
Chemické a fyzikálne vlastnosti izotopov
V neutrálnom atóme sa počet elektrónov rovná počtu protónov, takže izotopy toho istého prvku majú rovnakú elektrónovú štruktúru. Preto sú izotopy chemicky takmer nerozlíšiteľné — ich väzby a reakčná schopnosť sú veľmi podobné. Fyzikálne vlastnosti (ako je hmotnosť, hustota, rýchlosť difúzie, vibrácie v molekulách) sa však líšia.
Rozdiely v reakčných rýchlostiach medzi izotopmi sa nazývajú kinetický izotopový efekt alebo všeobecne hmotnostný efekt. Ťažšie izotopy reagujú spravidla pomalšie než ľahšie, pri čom je tento efekt najvýraznejší pri ľahkých prvkoch — najznámejšie pri protóniu a deutériu, kde má deutérium približne dvojnásobnú hmotnosť oproti protóniu. U ťažších prvkov je rozdiel relatívnych atómových hmotností medzi izotopmi menší, a teda aj hmotnostný efekt obyčajne malý.
Stabilné a rádioaktívne izotopy
Niektoré izotopy sú stabilné (nevykazujú rádioaktívny rozpad), iné sú rádioaktívne a spontánne sa rozpadávajú na iné nuklidy vyžarovaním častíc alebo fotónov. Rádioaktívne rozpady môžu mať rôzne mechanizmy: alfa rozpad, beta rozpad (β− alebo β+), zachytenie elektrónu alebo spontánne štiepenie. Každý rádioaktívny izotop má charakteristický polčas rozpadu (half‑life), ktorý môže byť od zlomkov sekundy až po miliardy rokov.
Rádioaktívne izotopy môžu byť prirodzené (napr. uhlík‑14 vzniká v atmosfére pri kozmickom žiarení) alebo umelo vyrobené v reaktoroch či urýchľovačoch častíc.
Energetika jadra a hmotnostný defekt
Nukleárna stabilita a energetika súvisia s pojmom väzobná energia jadra. Súčet hmotností jednotlivých nukleónov je väčší než hmotnosť hotového jadra; rozdiel sa nazýva hmotnostný defekt a podľa Einsteinovej rovnice E = mc2 sa pretvára na väzobnú energiu, ktorá drží jadro pohromade. Variácie v tejto väzobnej energii medzi izotopmi vysvetľujú, prečo niektoré nuklidy sú stabilné a iné majú sklony k rozpadu.
Praktické využitia izotopov
- Datovanie: rádioaktívne izotopy ako uhlík‑14 (14C) sa používajú na určovanie veku archeologických nálezov a geologických vzoriek.
- Medicína: rádioizotopy slúžia v diagnostike a terapii — napr. technécium‑99m v nukleárnej medicíne, fluor‑18 v PET snímkovaní.
- Energetika: izotopy uránu a plutónia sú palivom v jadrových reaktoroch; separácia izotopov (napr. obohacovanie uránu) je kľúčová pre ich použitie.
- Vedecký výskum a sledovanie: izotopické značkovanie (tracery) umožňuje sledovať chemické, biologické a ekologické procesy bez rušenia systému.
- Paleoklimatológia a geológia: pomer izotopov kyslíka (O‑16/O‑18) alebo izotopy vodíka v ľadových jadrách pomáhajú rekonštruovať staré klimatické podmienky.
Separácia izotopov a prirodzené zloženie
Izotopy toho istého prvku sa často v prírode vyskytujú v určitých relatívnych zastúpeniach (prírodné zastúpenie). Pre priemyselné či vedecké účely je niekedy potrebné izotopy separovať alebo obohatiť — používa sa centrifugácia plynov, difúzna separácia, destilácia, elektromagnetické metódy alebo laserové techniky. Tieto procesy sú technicky náročné, pretože izotopy sa fyzikálne líšia len veľmi málo.
Zhrnutie
Izotopy sú varianty atómov toho istého prvku s rovnakým počtom protónov, ale rôznym počtom neutrónov. Majú rovnaké chemické vlastnosti (vďaka identickej elektronovej štruktúre), no líšia sa fyzikálne — predovšetkým hmotnosťou, stabilitou a jadrovými vlastnosťami. Ich štúdium a využitie má zásadný význam v chémii, fyzike, medicíne, archeológii, geológii a ďalších oblastiach.