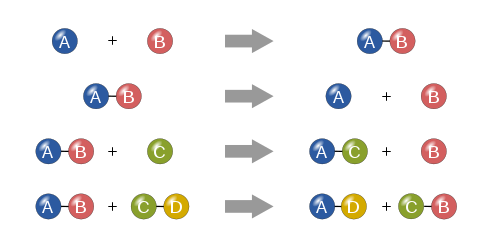
Chemická reakcia nastáva vtedy, keď sa jedna alebo viac chemických látok zmení na jednu alebo viac iných chemických látok. Príklady:
- železo a kyslík sa spájajú a vytvárajú hrdzu
- ocot a jedlá sóda sa spoja na octan sodný, oxid uhličitý a vodu
- horiace alebo vybuchujúce veci
- mnohé reakcie, ktoré prebiehajú v živých organizmoch.
- elektrochemické reakcie pri vybíjaní alebo nabíjaní batérií
Niektoré reakcie sú rýchle a iné pomalé. Niektoré prebiehajú rôznou rýchlosťou v závislosti od teploty alebo iných faktorov. Napríklad drevo nereaguje so vzduchom, keď je studené, ale ak sa dostatočne zahreje, začne horieť. Pri niektorých reakciách sa uvoľňuje energia. Ide o exotermické reakcie. Pri iných reakciách sa energia prijíma. Ide o endotermickéreakcie.
Jadrové reakcie nie sú chemické reakcie. Chemické reakcie zahŕňajú len elektróny atómov, jadrové reakcie zahŕňajú protóny a neutróny v atómových jadrách.
Rozšírenie: čo presne chemická reakcia znamená
Pri chemickej reakcii dochádza k preradeniu väzieb medzi atómami a k prestaveniu elektrónov okolo jadier. Po reakcii vznikajú látky s inými chemickými a často aj fyzikálnymi vlastnosťami (napr. farba, bod topenia, rozpustnosť). Základným zákonom je zákon zachovania hmoty — počet atómov každého prvku pred reakciou sa rovná počtu atómov po reakcii, preto chemické rovnice musia byť vyvážené.
Hlavné typy chemických reakcií (s príkladmi)
- Synthéza (súhrnné reakcie): dva alebo viac reaktantov tvoria jeden produkt. Príklad: 2 H₂ + O₂ → 2 H₂O (tvorba vody).
- Rozklad (dekompozícia): zlúčenina sa rozpadá na jednoduchšie látky. Príklad: CaCO₃ → CaO + CO₂ (tepelný rozklad vápenca).
- Náhrada (jednoduchá alebo substitučná): atóm alebo ión v zlúčenine je nahradený iným. Príklad: Zn + 2 HCl → ZnCl₂ + H₂.
- Metatéza (dvojitá výmena): ióny medzi dvoma zlúčeninami si vymenia miesto. Príklad: Na₂SO₄ + BaCl₂ → BaSO₄ (zrazenina) + 2 NaCl.
- Spálenie (kompletne exotermická oxidácia): organické látky reagujú s O₂ a vznikajú CO₂ a H₂O (ak je dostatok kyslíka). Príklad: CH₄ + 2 O₂ → CO₂ + 2 H₂O.
- Redox reakcie: reakcie, pri ktorých dochádza k prenosu elektrónov (oxidácia a redukcia). Napríklad pri korózii železa jedno z rekcií zahŕňa prenos elektrónov medzi Fe a O₂.
- Kyselina–zásada (protónové výmenné reakcie): HCl + NaOH → NaCl + H₂O (neutralizácia).
- Precipitačné reakcie: vznik nerozpustnej látky (zrazeniny), napr. pri miesení vhodných roztokov iónov.
- Polymerizácia a kopolymerizácia: malé molekuly (monoméry) sa spájajú do veľkých makromolekúl (polymérov).
Rýchlosť reakcie a faktory, ktoré ju ovplyvňujú
Rýchlosť chemickej reakcie určuje, ako rýchlo sa menia koncentrácie reaktantov a produktov v čase. Medzi hlavné faktory patria:
- Teplota: zvýšenie teploty zvyčajne zvyšuje rýchlosť reakcie (častice majú viac kinetickej energie a častejšie prekonávajú aktivačnú energiu).
- Koncentrácia reaktantov: vyššia koncentrácia zvyšuje počet zrážok medzi časticami za jednotku času.
- Povrchová plocha: u pevných reaktantov väčší povrch (napr. prášok vs kus) zvyšuje rýchlosť reakcie.
- Katalyzátory: látky, ktoré znižujú aktivačnú energiu a zrýchľujú reakciu bez toho, aby sa samy trvalo spotrebovali. V biologických systémoch to sú enzýmy.
- Tlak (u plynov): zvýšenie tlaku efektívne zvyšuje koncentráciu plynov a môže zrýchliť reakciu.
Energetika reakcií
Energetické aspekty opisujú, či sa pri reakcii energia uvoľňuje alebo spotrebúva:
- Exotermické reakcie: uvoľňujú teplo do okolia (produkty majú nižšiu entalpiu než reaktanty). Príklad: spaľovanie dreva alebo benzínu.
- Endotermické reakcie: vyžadujú príjem energie zo okolia, aby prebehli (produkty majú vyššiu entalpiu). Príklad: rozklad uhličitanu vápenatého pri zahriatí.
Ďalšie dôležité pojmy: aktivačná energia (energie, ktorú musia častice prekonať, aby reakcia prebehla) a entalpia (H), ktorá charakterizuje tepelné zmeny pri konštantnom tlaku. Kinetika (rýchlosť) a termodynamika (možnosť a energetická výhodnosť) sú dve rôzne oblasti popisu reakcií — nie každá termodynamicky možná reakcia prebehne rýchlo bez vhodného katalyzátora alebo dodania energie.
Chemické rovnice a stechiometria
Chemická rovnica zapisuje reaktanty a produkty a často aj pomer, v ktorom reagujú. Predpisy pre správnu prácu s rovnicami:
- rovnice treba vyvážiť tak, aby bol zachovaný počet atómov každého prvku;
- stechiometria umožňuje vypočítať množstvá reaktantov a produktov (napr. koľko látky vznikne z určitého množstva východiskovej látky);
- pri plynoch sa často používajú vzťahy podľa molárnych objemov pri danej teplote a tlaku, pri roztokoch zase koncentrácie (molárna, hmotnostná ap.).
Reverzibilita a chemická rovnováha
Mnohé reakcie sú reverzibilné — prebiehajú v oboch smeroch. Po čase sa môže nastaviť stav, keď rýchlosť priebehu dopredu sa rovná rýchlosti priebehu dozadu; tomu hovoríme chemická rovnováha. Poloha rovnováhy sa dá ovplyvniť podľa Le Chatelierovho princípu zmenou koncentrácie, teploty alebo tlaku (u plynov). Rovnováha sa kvantifikuje pomocou rovnovážnej konštanty K.
Bezpečnosť a praktické príklady
Chemické reakcie môžu byť užitočné aj nebezpečné. Pri manipulácii s reaktívnymi látkami treba brať do úvahy možnosť uvoľnenia tepla, výbuchu, tvorby toxických plynov alebo korózie materiálov. V priemysle a laboratóriách sa používajú bezpečnostné postupy: ochranné pomôcky, vetranie, kontrola teploty a tlaku, neutralizácia odpadov.
Praktické príklady v bežnom živote: varenie (varenie je súbor chemických a fyzikálnych zmien), čistenie (reakcie bielidiel, enzýmov v pracích prostriedkoch), výroba energie v batériách (elektrochemické reakcie), farmaceutické syntézy, poľnohospodárske hnojivá, a biochemické reakcie v bunkách (enzýmom katalyzované procesy).
Ak máte záujem, môžem pridať vyvážené chemické rovnice ku konkrétnym príkladom (napr. hrdza, neutralizácia octu a jedlej sódy, alebo reakcie v batérii) a vysvetliť ich krok po kroku.