Elektrón je veľmi malý kúsok hmoty a energie. Jeho symbol je e−. Objavil ho J. J. Thomson v roku 1897 pri experimentoch s katódovými lúčmi; meral pomer náboja k hmotnosti (e/m) a ukázal, že tieto lúče pozostávajú z častíc menších než atóm.
Vlastnosti
Elektrón je subatomárna častica a predpokladá sa, že je elementárnou časticou, teda sa nedá ďalej rozložiť na menšie častice. Niektoré dôležité fyzikálne vlastnosti:
- Elektrický náboj: záporný, s veľkosťou približne 1,602176634×10−19 C (elementárny náboj).
- Hmotnosť: veľmi malá, pokojová hmotnosť približne 9,10938356×10−31 kg (alebo ~0,511 MeV/c2 v energetických jednotkách).
- Spin: 1/2 — je fermiónom a riadi sa Pauliho vylučovacím princípom a Fermiho–Diracovou štatistikou.
- Magentický moment: vlastný magnetický moment spôsobený spinom; jeho presné meranie patrí medzi testy kvantovej elektrodynamiky (QED).
- Rýchlosť: môže sa pohybovať veľmi vysokými rýchlosťami, blízkymi rýchlosti svetla, pričom pri vysokých rýchlostiach treba uvažovať relativistické efekty.
- Vlnovo-časticové správanie: prejavuje sa dualitou vlna–častica (de Broglieova vlnová dĺžka), čo je dôležité napr. pri elektronovej mikroskopii.
Interakcie
Elektróny sa zúčastňujú na viacerých základných interakciách:
- gravitačnej (veľmi slabá pri úrovni elementárnych častíc),
- elektromagnetickej (najvýznamnejšia pre správanie elektrónov — určuje elektrické a magnetické sily medzi nimi a inými nabitými časticami),
- slabej interakcii (účasť pri rádioaktívnom beta rozpade a ďalších procesoch).
Elektrická energia, ktorá poháňa televízory, motory, mobilné telefóny a mnoho ďalších zariadení, je v podstate prúdom elektrónov pohybujúcich sa po drôtoch alebo iných vodičoch. V kovoch sú viazané elektróny valenčnej vrstvy zodpovedné za vedenie elektrického prúdu.
Úloha v atóme a v chémii
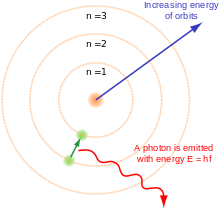
V atómoch elektróny obiehajú okolo jadra v kvantovo definovaných stavoch (orbitáloch) charakterizovaných kvantovými číslami. Počet a usporiadanie valenčných elektrónov určujú chemické vlastnosti prvku, väzby medzi atómami (kovalentné, iónové, kovové) a reakčnú schopnosť. Ionizácia znamená odtrhnutie elektrónu z atómu, čo vytvára ión.
Objav, vývoj teórií a príbuzné javy
Po Thomsonovom objave nasledovali ďalšie významné kroky: Millikanove merania náboja elektrónu (olieňový experiment), kvantová mechanika, ktorá vysvetlila štandardné modely atómových hladín, a Diracova rovnice, ktorá predpovedala existenciu pozitívne nabitej antiparty — pozitronu (objavený A. H. Andersonom v roku 1932). Moderné teórie, najmä kvantová elektrodynamika (QED), opisujú presné interakcie elektrónov s elektromagnetickým poľom.
Použitie
Elektróny majú obrovský praktický význam v technike a vede:
- Elektronika: sú nosičmi prúdu v polovodičoch, tranzistoroch, integrovaných obvodoch a iných súčiastkach.
- Elektrónové mikroskopy: využívajú vlnové vlastnosti elektrónov na zobrazovanie s rozlíšením omnoho vyšším než možné s optickým mikroskopom.
- Röntgenové žiarenie a lampy: rýchle elektróny dopadajúce na kovové terče produkujú röntgenové žiarenie.
- Urýchľovače častíc a detektory: štúdium elementárnych častíc a vysokých energií využíva zväzky elektrónov (a pozitronov).
- Moderné aplikácie: LED, solárne články, spintrónika (využitie spinu elektrónov), elektronové lúče v priemyselnom spracovaní a medicíne.
Elektrón je teda kľúčová častica pre pochopenie štruktúry hmoty, fungovania elektrických a elektronických zariadení a mnohých javov v modernej fyzike a technike.