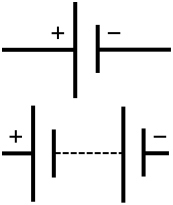Batéria premieňa chemickú energiu na elektrickú energiu pomocou chemickej reakcie. Chemické látky (reaktanty) sú uložené vo vnútri batérie medzi dvoma elektródami a elektrolytom; pri reakcii sa uvoľňujú elektróny, ktoré tečú vonkajším obvodom a napájajú iné komponenty pripojené v obvode. Batéria produkuje jednosmerný elektrický prúd (DC), teda prúd, ktorý tečie jedným smerom. V mnohých situáciách je použitie elektrickej siete lacnejšie a efektívnejšie, no batérie sú nenahraditeľné tam, kde nie je dostupný rozvod elektrickej energie alebo kde sa vyžaduje mobilita — napríklad v elektrických vozidlách a v mobilných telefónoch.
Princíp fungovania
Batéria pozostáva z dvoch elektród (anóda a katóda) a elektrolytu. Počas vybíjania prebieha redoxná reakcia: anóda sa oxiduje (uvoľňuje elektróny) a katóda sa redukuje (prijíma elektróny). Elektróny pretekajú z anódy do katódy cez vonkajší obvod, zatiaľ čo ióny putujú vnútri batérie cez elektrolyt, aby sa udržala elektroneutralita. Rozdiel potenciálov medzi elektródami určuje napätie článku.
Stavebné časti batérie
- Anóda – záporná elektróda pri vybíjaní (materiál, ktorý uvoľňuje elektróny).
- Katóda – kladná elektróda pri vybíjaní (prijíma elektróny).
- Elektrolyt – látka (kvapalina, gél alebo pevná látka), ktorá umožňuje pohyb iónov medzi elektródami.
- Separator – porézna bariéra, ktorá zabraňuje skratu medzi elektródami, ale umožňuje priechod iónov.
- Kontajner a svorky – mechanické a elektrické súčasti zabezpečujúce pripojenie a ochranu článku.
- Ochranné prvky (napr. ventil, BMS) – najmä v dobíjateľných batériách sa používajú na kontrolu nabíjania, meranie napätia a prúdu a prevenciu prehriatia či skratu.
Typy batérií: primárne a sekundárne
Batérie môžu byť primárne alebo sekundárne. Primárna batéria je jednorazová — keď sa vybije, už sa nenabíja a zvyčajne sa vyhodí (alebo recykluje). Typickými príkladmi sú alkalické články (AA, AAA) a niektoré lítiové gombíkové články (napr. CR2032). Sekundárna batéria je dobíjateľná a možno ju použiť opakovane po nabití; sem patria olovené akumulátory, NiMH, NiCd a moderné lítiovo-iónové (Li-ion) články.
- Primárne (jednorazové) – výhody: dlhá skladovateľnosť, nízke samovybíjanie, jednoduché použitie. Nevýhody: jednorazové použitie, tvorba odpadu.
- Sekundárne (dobíjateľné) – výhody: opakované použitie, nižšie prevádzkové náklady pri dlhodobom používaní; nevýhody: potreba nabíjačky, obmedzený počet nabíjacích cyklov, citlivosť na nesprávne nabíjanie (u niektorých typov).
Bežné chemické systémy
- Alkalické (primárne) – bežné pre diaľkové ovládače, hračky.
- Vymeniteľné lítiové gombíkové články (primárne) – hodinky, kalkulačky, niektoré senzory.
- Olovenné akumulátory (Pb) – autobatérie, UPS; nízke náklady, vysoký prúdový výkon, ale nižšia energetická hustota a vyššia hmotnosť.
- NiCd a NiMH (sekundárne) – použité v nástrojoch, starších prenosných zariadeniach; NiCd má problém s pamäťovým efektom, NiMH má vyššiu kapacitu.
- Lítiovo-iónové a lítiovo-polymérové (Li-ion, LiPo) (sekundárne) – vysoká energetická hustota, bežné v smartfónoch, notebookoch a elektrických vozidlách.
Kapacita, napätie a ďalšie parametre
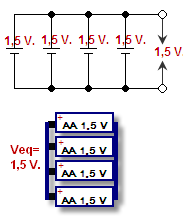
Kapacita batérie sa meria v ampérhodinách (Ah) alebo miliampérhodinách (mAh) a udáva, koľko náboja môže batéria dodať pri určitej záťaži. Nominalné napätie závisí od chemického systému (napr. alkalický článok ~1,5 V, olovený ~2,0 V na článok, Li-ion ~3,6–3,7 V na článok). Pre dosiahnutie vyššieho napätia alebo kapacity sa články spájajú do sĺupcov (séria pre vyššie napätie, paralelne pre vyššiu kapacitu). Dôležité sú aj vnútorný odpor, výkonová hustota a rýchlosť nabíjania/vybíjania (C-rate).
Nabíjanie a údržba (sekundárne batérie)
- Nabíjacie metódy sa líšia podľa typu: napr. Li-ion sa nabíjajú režimom CC‑CV (konštantný prúd, potom konštantné napätie), olovené majú špeciálne záverečné nabíjanie a vyrovnávacie cykly.
- Pre bezpečnosť a dlhú životnosť je dôležitý BMS (Battery Management System), ktorý kontroluje napätie jednotlivých článkov, teplotu a prúd.
- Vyhýbajte sa hlbokému vybijaniu (u niektorých typov) a prehriatiu; nesprávne nabíjanie môže viesť k zníženiu kapacity alebo k nebezpečným stavom (napr. tepelná runaway u Li-ion).
Bezpečnosť a životné prostredie
Batérie obsahujú chemikálie a ťažké kovy, ktoré môžu byť nebezpečné pri nesprávnom zaobchádzaní. Dôležité zásady:
- Zabraňte skratu medzi svorkami (krátke spojenie môže spôsobiť iskrenie a požiar).
- Nepoužívajte poškodené alebo nafúknuté batérie; pri podozrení na poškodenie ich bezpečne zlikvidujte.
- Recyklujte batérie podľa miestnych predpisov — mnohé druhy (najmä olovené a Li-ion) sú recyklovateľné a separované zberné miesta znižujú environmentálnu záťaž.
- Těžba surovín (napr. lítium, kobalt) má environmentálne a sociálne dopady; preto rastie záujem o recykláciu a vývoj batérií s menším podielom vzácnych alebo toxických prvkov.
Použitie
- Prenosné elektronické zariadenia: mobilné telefóny, notebooky, tablety, fotoaparáty.
- Doprava: elektrické vozidlá, e-biky, skútre.
- Záložné zdroje a sieťové úložiská energie (UPS, systémy pre obnoviteľné zdroje).
- Domáce a priemyselné aplikácie: nástroje, signalizačné zariadenia, meracia technika, lekárske prístroje.
- Off-grid použitia a mobilné napájanie tam, kde nie je dostupná rozvod elektrickej energie.
Správny výber typu batérie závisí od požiadaviek na energiu, hmotnosť, veľkosť, cenu, počet cyklov a bezpečnosť. Pri vývoji a nasadení batériových systémov sa kladie dôraz na účinnosť, ekologický dopad a bezpečnosť používateľov.