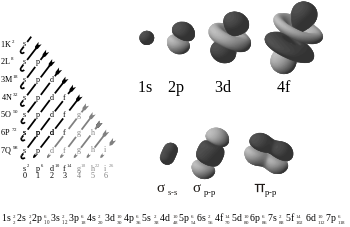
V chémii sú väzby typu pi (π väzby) kovalentné chemické väzby, v ktorých sa dráha jedného elektrónu križuje (prekrýva) s dráhou iného elektrónu. Elektróny majú dráhu v tvare laloku osmičky (pozri obrázok). Existujú dve oblasti prekrývania, pretože dráhy sa prekrývajú na oboch lalokoch. Iba jedna z uzlových rovín orbitalu prechádza oboma zúčastnenými jadrami.
Grécke písmeno π v ich názve označuje p orbitály. Symetria orbitálu väzby pi vyzerá rovnako ako orbitál p pri pohľade na os väzby. P orbitály majú zvyčajne tento druh väzby. Predpokladá sa, že aj D orbitály využívajú väzbu pi, ale v skutočnosti sa tak nemusí nevyhnutne diať. Myšlienka väzbových d orbitálov zapadá do teórie hypervalencie.
Väzby pí sú zvyčajne slabšie ako väzby sigma. Kvantová mechanika hovorí, že je to preto, lebo dráhy orbitálov sú paralelné, takže sa p-orbitály oveľa menej prekrývajú.
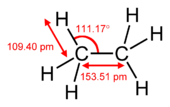
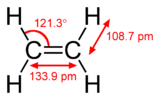
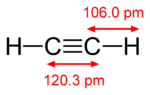
K väzbe pí dochádza, keď sa dva atómové orbitaly dotýkajú prostredníctvom dvoch oblastí prekrývania. Väzby pí sú viac rozptýlené ako väzby sigma. Elektróny vo väzbách pí sa niekedy nazývajú elektróny pí. Molekulové fragmenty spojené väzbou pí sa nemôžu otáčať okolo tejto väzby bez porušenia väzby pí. Rotácia zničí paralelné dráhy dvoch p orbitálov.