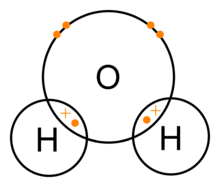
Kovalentné väzby sú chemické väzby medzi dvoma nekovovými atómami. Príkladom je voda, kde vodík (H) a kyslík (O) vytvárajú väzbu H2O. Plná vonkajšia škrupina má zvyčajne osem elektrónov alebo dva v prípade vodíka či hélia. Valenčné elektróny sú elektróny, ktoré sa vo vonkajšej škrupine atómu nachádzajú relatívne voľne a sú najdôležitejšie pri tvorbe väzieb. Štruktúru elektrónových obalov určuje kvantová mechanika.
Mechanizmus vzniku kovalentnej väzby
Kovalentná väzba vzniká, keď sa valenčné elektróny dvoch atómov zdieľajú tak, že dochádza k prekryvu ich atómových orbitálov a tvorbe spoločných molekulárnych orbitálov. Z tohto prekryvu vzniká väzbový (bonding) orbitál s nižšou energiou a často aj antibonding orbitál s vyššou energiou. Elektróny obsadia väzbové orbitály, čím sa systém energeticky stabilizuje a atómy sa navzájom priťahujú.
Príkladný mechanizmus možno opísať zjednodušene takto: ak sa atóm s voľným elektrónom priblíži k inému atómu s voľným elektrónom, ich atómové orbitály sa prekryjú a vytvoria spoločný orbitál viazaný na obe jadrá. Obsadením tohto orbitálu elektronmi sa zníži energia systému a vznikne väzba. Uvoľnená energia pri tvorbe väzby sa môže vydať napríklad ako tepelná energia alebo fotón, hoci pri chemických reakciách je bežnejšie, že energia prejde do vibračných či rotačných stupňov slobody molekuly.
Typy kovalentných väzieb
- Jednoduchá väzba – zdieľanie jedného páru elektrónov (napr. H–H v H2).
- Dvojitá väzba – zdieľanie dvoch párov elektrónov (napr. O=O v O2); pozostáva z jednej sigma a jednej pi väzby.
- Trojitá väzba – zdieľanie troch párov elektrónov (napr. N≡N v N2); pozostáva z jednej sigma a dvoch pi väzieb.
- Sigma (σ) a pi (π) väzby – sigma vzniká pri priamom prekrývaní orbitálov pozdĺž osi medzi jadrami; pi vzniká bočným prekrývaním p-orbitálov a je slabšia než sigma.
- Koordinačná (donor‑akceptorová, dative) väzba – oba elektróny zdieľa len jeden atóm (napr. v komplexoch, alebo pri tvorbe NH4+).
Polarita kovalentnej väzby
Väzba môže byť nepolarizovaná (nerozdelené zdieľanie elektrónov) alebo polárna (elektróny sú viac priťahované jedným z atómov). Rozdiel určuje elektronegativita atómov. Keď jeden atóm priťahuje väzbový pár silnejšie, vznikajú čiastočné náboje: δ− pri elektrone‑prijímajúcom atóme a δ+ pri elektrone‑odovzdávajúcom atóme. Takéto čiastočné náboje vedú k elektrostatickej príťažlivosti medzi atómami a môžu spôsobiť, že molekula bude polárna (napr. molekula voda, kde kyslík je δ− a vodíky sú δ+).
Geometria a hybridizácia
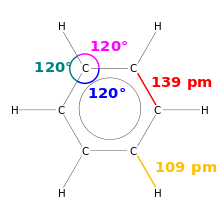
Priestorové usporiadanie atómov v molekule súvisí s hybridizáciou atómových orbitálov (napr. sp, sp2, sp3) a s počtom väzieb a voľných elektronových párov. Hybridizácia vysvetľuje typické uhly a tvary: napríklad sp3 vedie k tetraedrickej geometrii (CH4), sp2 k rovinnému trigonom (C2H4), a sp k lineárnej geometrii (C≡C).
Vlastnosti kovalentných väzieb
- Dĺžka väzby – vzdialenosť medzi jadrami viazaných atómov; kratšie väzby sú zvyčajne silnejšie.
- Energie väzby – energia potrebná na roztrhnutie väzby (dissociačná energia); viacnásobné väzby majú obyčajne vyššiu celkovú energiu na atómový pár, pričom jednotková energia na jeden zdieľaný pár môže variovať.
- Elektrická vodivosť – väčšina molekulárnych zlúčenín s kovalentnými väzbami je zlým vodičom elektriny v pevnom stave (s výnimkami, napr. aromatické vodivé materiály).
- Typ materiálu – kovalentné väzby môžu tvoriť diskrétne molekuly (H2O, CO2) alebo sieťové (diamant, SiO2), ktoré majú veľmi vysoké teploty topenia a tvrdosť.
Príklady
- H2: jednoduchá nepolárna väzba medzi dvoma vodíkmi.
- Cl2: jednoduchá nepolárna väzba medzi dvoma chlórovými atómami.
- O2: dvojitá väzba medzi atómami kyslíka (paramagnetická kvôli nespárovaným elektrónom v molekulárnych orbitáloch).
- N2: trojitá väzba, veľmi silná a krátka (dôležitá v atmosfére).
- Voda, H2O: kyslík zdieľa po jednom páre elektrónov s každým vodíkom, výsledkom je polarita molekuly a zahýbený tvar s uhlom približne 104,5°.
- CO2: lineárna molekula s dvojnými väzbami C=O; celkovo nepolárna, hoci jednotlivé C=O väzby sú polárne.
- CH4 (metán): sp3 hybridizácia uhlíka, tetraedrický tvar, nepolárna molekula.
Oktetové pravidlo a výnimky
Octet rule (pravidlo ôsmich elektrónov) pomáha vysvetliť mnoho kovalentných väzieb u prvkov druhej periody. Existujú však výnimky:
- molekuly s nepárnym počtom elektrónov (radikály), napr. NO;
- nedostatočná octeta, napr. BF3, kde bor má 6 valenčných elektrónov;
- rozšírená octeta u väčších atómov (P, S, Cl), napr. SF6.
Rozdiel medzi kovalentnou a iónovou väzbou
Kovalentná väzba vzniká z delenia elektrónov medzi atómami, zatiaľ čo iónová väzba vzniká prenosom elektrónu z jedného atómu na druhý a následnou elektrostatickou príťažlivosťou medzi opačne nabitými iónmi. V praxi existuje kontinuum medzi čistou iónovou a čistou kovalentnou väzbou — mnohé väzby sú čiastočne iónové v dôsledku rozdielu elektronegativity.
Lámavanie a energetika väzieb
Aby sa kovalentná väzba prerušila, je potrebné dodať energiu približne rovnakú, aká sa uvoľnila pri jej vzniku (konkrétna hodnota závisí od typu väzby). Chemické reakcie prebiehajú tak, že sa najprv rozbijú niektoré väzby (spotreba energie) a potom vzniknú nové väzby (uvoľnenie energie). Rozdiel týchto energií určuje, či je reakcia exotermická alebo endotermická.
Zhrnutie
Kovalentná väzba je základným mechanizmom, ktorým sa spájajú atómy nekovov do molekúl a sieťových štruktúr. Rozsah kovalentného charakteru, typ väzby (σ, π), polarita, geometria a energetika určujú chemické a fyzikálne vlastnosti látky — od jednoduchých plynov až po pevné, veľmi tvrdé sieťové kryštály ako diamant.