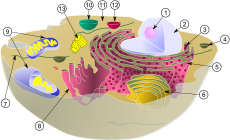
V bunkovej biológii je centrozóm organelou, ktorá je hlavným miestom organizácie bunkových mikrotubulov. Reguluje tiež cyklus bunkového delenia, teda fázy, ktoré vedú k rozdeleniu jednej bunky na dve.
Centrozóm objavil Edouard Van Beneden v roku 1883 a v roku 1888 ho opísal a pomenoval Theodor Boveri.
Centrozóm sa zrejme vyvinul len v živočíšnych bunkách. Huby a rastliny používajú na usporiadanie svojich mikrotubulov iné štruktúry. Hoci centrozóm zohráva kľúčovú úlohu pri efektívnej mitóze v živočíšnych bunkách, nie je nevyhnutný.
Centrozóm sa skladá z dvoch centriol, ktoré sú navzájom v pravom uhle. Sú obklopené beztvarou hmotou bielkovín.
Stavba centrozómu
Centrozóm tvorí dve centrioly (zvyčajne jedna materská a jedna dcérska), ktoré sú usporiadané tak, že ich osi sú na seba kolmé. Každá centrióla je valcovitá štruktúra zložená typicky z deviatich trojíc mikrotubulových pražcov (tzv. 9×3 usporiadanie). Centrioly majú obvykle dĺžku rádovo stovky nanometrov a sú obklopené amorfnou pericentrionálnoou hmotou (PCM — pericentriolárna hmota), ktorá obsahuje množstvo proteínov nevyhnutných pre nukleáciu mikrotubulov.
Medzi dôležité proteíny v PCM patria γ-tubulín (gamma-tubulín), ktorý tvorí γ-TuRC (γ-tubulin ring complex) — „základňu“ pre tvorbu nových mikrotubulov, ďalej pericentrín (pericentrin), CEP proteíny (napr. CEP192) a ďalšie faktory, ktoré regulujú počet a stabilitu mikrotubulov.
Funkcie centrozómu a mikrotubulov
- Organizácia mikrotubulového cytoskeletu — centrozóm funguje ako hlavn é MTOC (microtubule-organizing center), odkiaľ sa núklujú mikrotubuly a formuje sa radiálna sieť v interfáze.
- Účasť pri delení buniek — počas G2/M fázy sa centrozómy „dozrejú“ (centrosome maturation), zväčší sa PCM a zvýši sa schopnosť nukleovať mikrotubuly, čo vedie k vytvoreniu dvoch pólov mitotického vretena.
- Orientácia vretena a polarita bunky — centrozómy pomáhajú orientovať mitotické vreteno, čo je dôležité pri asymetrickom delení kmeňových buniek a pri udržiavaní bunkovej polarity.
- Vytváranie cilíí a bičíkov — centrioly sa môžu diferencovať na bazálne teliesko (bazálne telo), ktoré iniciuje rast primárnych cilíí alebo bičíkov.
Cyklus centrozómu a jeho regulácia
Centrozóm sa duplikuje raz za bunkový cyklus, obvykle začínajúc v S-fáze. Počas duplikácie vzniká k novej centrioly tzv. „procentriole“, orientovaná kolmo k existujúcej centriole. Regulácia duplikácie zahŕňa viacero kľúčových proteínov, medzi ktoré patrí enzým PLK4 (Polo-like kinase 4), SAS-6, STIL a ďalšie. Presné načasovanie a mechanizmy „licencovania“ zabraňujú viacnásobnej duplikácii v jednom cykle.
Pri prechode do mitózy nastupuje centrosome maturation: do PCM sa navyše nahrnie množstvo faktorov, čo zvyšuje počty nukleovaných mikrotubulov a pomáha vytvoriť silné dvojpólové mitotické vreteno. Separácia centrozómov do opačných pólov bunky je sprostredkovaná motorovými proteínmi (napr. kinesín-5) a silami v cytoskeletoch.
Centrozóm nie je jediná cesta k deleniu
Aj keď je centrozóm hlavným MTOC u väčšiny živočíšnych buniek, bunky dokážu za určitých okolností vytvoriť funkčné mitotické vreteno aj bez centrumzómu. Existujú mechanizmy založené na chromatinom riadenej nukleácii mikrotubulov (Ran-GTP gradient), augminovom komplexe a microtubule-mediated nucleation, ktoré môžu kompenzovať stratu centrozómu. Preto sú experimentálne bunky bez centrozómov schopné deliť sa, hoci často s nižšou efektivitou a vyšším rizikom chýb (napr. multipolárne delnie).
Evolučné rozdiely a variácie
Centrozóm sa zrejme vyvinul v živočíšnych líniách; mnoho rastlinných a plesňových buniek používa iné organizátory mikrotubulov. Napríklad kvasinky majú špecifickú štruktúru nazývanú spindle pole body, ktorá plní analógickú funkciu oproti centrozómu. U niektorých organizmov môže dochádzať k de novo biogenéze centriól v embryách alebo pri špecifických vývojových štádiách.
Klinický význam a patológia
- Rakovina: nárast počtu centrozómov (centrosome amplification) je často spojený s genomickou nestabilitou a agresívnejším priebehom nádorov, pretože viacero centrozómov môže viesť k multipolárnemu vretenu a chybám v segregácii chromozómov.
- Rozvojové poruchy: mutácie v génoch kódujúcich centrosomálne proteíny (napr. ASPM, CENPJ/CENP-J, CEP152) môžu viesť k mikrocefálii a iným neurovývojovým ochoreniam.
- Ciliopatie: poškodenie alebo chybná funkcia bazálnych teliesok (odvozených od centriól) vedie k chorobám spojeným s nefunkčnými ciliami — poruchy zraku, obličiek, respiračného epitelu a ďalšie symptómy.
Metódy štúdia
Centrozómy a centrioly sa skúmajú pomocou rôznych techník: elektronová mikroskopia odhaľuje ultrastruktúru centriól, imunofluorescencia s protilátkami proti γ-tubulínu alebo pericentrínu značí pozíciu centrozómu v bunke a živé zobrazovanie umožňuje sledovať duplikáciu a separáciu v reálnom čase. Molekulárne genetické prístupy (CRISPR, RNAi) pomáhajú identifikovať funkcie jednotlivých centrosomálnych proteínov.
Centrozóm tak zostáva kľúčovým prvkom bunkovej organizácie a delenia — komplexný, dynamický a regulovaný systém, ktorého poruchy majú významné biologické a klinické dôsledky.