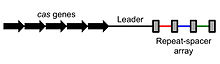
CRISPR je termín používaný v mikrobiológii. Je to skratka pre Clustered Regularly-Interspaced Short Palindromic Repeats (pravidelne rozmiestnené krátke palindromické repetície). Ide o prirodzený segment genetického kódu, ktorý sa nachádza u prokaryotov: má ho väčšina baktérií a archeí.
CRISPR má veľa krátkych opakujúcich sa sekvencií. Tieto sekvencie sú súčasťou adaptívneho imunitného systému prokaryotov. Umožňuje im zapamätať si a čeliť iným organizmom, ktoré ich lovia, napríklad bakteriofágom.
Majú potenciál modifikovať gény takmer každého organizmu. Sú súčasťou nástroja, ktorý umožňuje presne cielené rezanie a vkladanie génov pri genetickej modifikácii (GM). Pracuje sa na tom, aby sa zistilo, ako ich možno použiť na útok proti vírusovým ochoreniam u ľudí.
Ako CRISPR funguje v baktériách a archeách
CRISPR systém funguje ako pamäť a obranný mechanizmus v troch hlavných krokoch:
- Akvizícia (zachytenie): keď vírus (fág) infikuje bunku, časť jeho DNA môže byť vložená medzi repetície CRISPR ako tzv. spacer. Tento spacer slúži ako molekulárna „fotografia“ útočníka.
- Expresia: z CRISPR oblasti sa transkribujú krátke RNA (pre-crRNA), ktoré sa následne spracujú na jednotlivé crRNA obsahujúce spacer. Tieto crRNA sú naviazané na proteíny z rodiny Cas.
- Interferencia: keď sa rovnaký vírus znovu objaví, crRNA rozpozná zodpovedajúcu sekvenciu v jeho DNA a Cas proteín rozštiepi cudzí genóm, čím ho neutralizuje.
Hlavné komponenty systému
- Repetície (repeats) — krátke palindromické sekvencie pravidelne opakované.
- Spacery — unikátne sekvencie medzi repetíciami, odvodené od genetického materiálu predchádzajúcich invázorov.
- Cas proteíny (CRISPR-associated) — enzýmy, ktoré spracúvajú RNA, rozpoznávajú ciele a štiepia DNA alebo RNA. Najznámejší je Cas9.
- crRNA a guide RNA (gRNA) — RNA molekuly, ktoré vedú Cas enzým na konkrétnu cieľovú sekvenciu.
Typy CRISPR a enzýmy
Existuje niekoľko typov CRISPR systémov (označované I, II, III atď.), líšia sa zložením Cas proteínov a mechanizmom účinku. V biotechnológii sa najčastejšie používa systém typu II s enzýmom Cas9, ale populárne sú aj Cas12 a Cas13 (ten cieli RNA namiesto DNA).
CRISPR ako nástroj na editáciu génov
V genetickej editácii sa CRISPR/Cas používa takto (zjednodušene):
- Do bunky sa zaviedie Cas enzým spolu s navodzovacou RNA (gRNA), ktorá nasmeruje enzým na konkrétnu sekvenciu v genóme.
- Cas enzým vytvorí prerušenie (double-strand break) v cieľovej DNA.
- Pri oprave týchto prerušených miest bunkové mechanizmy môžu spôsobiť menšie zmeny (NHEJ — nepravidelné spájanie) alebo pri prítomnosti opravnej šablóny vnoriť konkrétnu zmenu (HDR — homológna opravná cesta).
Tento princíp umožňuje: vyraďovať gény, vkladať nové úseky DNA, opravovať mutácie alebo presne meniť bázy DNA s pomocou upravených variantov CRISPR (base editing, prime editing).
Aplikácie
- Výskum — rýchle generovanie génových mutácií a štúdium funkcie génov.
- Liečba genetických ochorení — ex vivo terapie (úprava pacientových buniek mimo tela) aj prvé pokusy in vivo (rovnaké bunky priamo v tele). Príklady klinických štúdií zahŕňajú terapie pre srdcové choroby, hemoglobinopatie (napr. srpkovitú anémiu) a dedičné očné choroby.
- Onkológia — upravené imunitné bunky (napr. CAR-T) zlepšujú rozpoznávanie a likvidáciu nádorových buniek.
- Pestovanie a šľachtenie plodín — rýchle zavádzanie žiadaných vlastností (odolnosť voči škodcom, zlepšenie výživovej hodnoty).
- Biotechnológia — výroba liečiv, vakcín, a presné úpravy mikroorganizmov pre priemyselné procesy.
Výhody a obmedzenia
- Výhody: jednoduché navádzanie na cieľ (stačí upraviť gRNA), vysoká účinnosť, možnosť súčasnej editácie viacerých miest (multiplexing), široké uplatnenie v rôznych organizmoch.
- Obmedzenia: riziko nepresných zásahov (off-target efekty), potreba vhodného PAM sekvenčného motívu pri cieli, ťažkosti s efektívnym a bezpečným doručením do buniek/tkanív, imunologické reakcie voči Cas proteínom, komplikácie pri editovaní zárodočných buniek (etické otázky).
Etika, bezpečnosť a regulácia
CRISPR otvára veľké možnosti, ale aj závažné etické dilemy. Editácia zárodočných buniek (germline) má potenciál meniť dedičné vlastnosti a vyvoláva obavy o dlhodobé dôsledky a spoločenské zmeny. Preto mnoho krajín pristupuje k regulácii prísne, klinické použitie najmä smeruje k liečbe somatických buniek (bez zmeny potomstva).
Záver
CRISPR predstavuje prirodzený adaptívny imunitný systém baktérií a archeí, ktorý vedcom poskytol výkonný nástroj pre genetickú editáciu. Jeho využitie prináša revolúciu v biomedicíne, poľnohospodárstve a výskume, avšak sprevádzajú ho technické výzvy a dôležité etické otázky, ktoré si vyžadujú zodpovedný prístup a jasnú reguláciu.