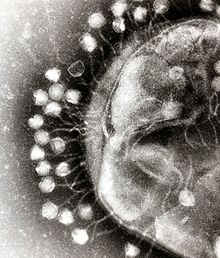
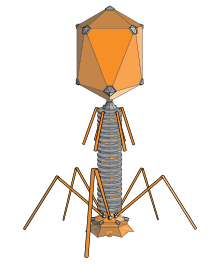
Bakteriofág je vírus, ktorý infikuje baktérie. Tento termín sa bežne skracuje na fág.
Bakteriofágy patria medzi najrozšírenejšie a najrozmanitejšie entity v biosfére. Podobne ako vírusy, ktoré infikujú eukaryoty (rastliny, živočíchy a huby), existuje mnoho rôznych štruktúr a funkcií fágov.
Fágy sa zvyčajne skladajú z vonkajšieho proteínového plášťa, ktorý obsahuje genetický materiál. Genetický materiál môže byť jednovláknový (ssRNA alebo ssDNA) alebo dvojvláknový (dsRNA alebo dsDNA). Môže byť dlhý 5 až 500 kilobázových párov s kruhovým alebo lineárnym usporiadaním. Bakteriofágy majú zvyčajne veľkosť od 20 do 200 nanometrov.
Genómy fágov môžu kódovať len štyri gény, ale aj stovky génov. Fágy vpravujú svoj genóm do baktérie a replikujú sa v nej.
Fágy sú všade, kde sa vyskytujú baktérie, napríklad v pôde alebo v črevách zvierat. V morskej vode sú veľmi rozšírené: v mikrobiálnych rohožiach na hladine sa našlo až 9 × 108 viriónov na mililiter a až 70 % morských baktérií môže byť infikovaných fágmi.
V bývalom Sovietskom zväze, v strednej Európe a vo Francúzsku sa ako alternatíva k antibiotikám používajú už viac ako 90 rokov. Ich skutočnú povahu však zistil až Helmut Ruska, ktorý v roku 1939 pozoroval prvý fág pod elektrónovým mikroskopom.
Sú možnou terapiou proti kmeňom mnohých baktérií odolných voči antibiotikám. Na druhej strane niektoré fágy komplikujú biofilmy pri pneumónii a cystickej fibróze. Chránia baktérie pred liekmi, a tak predlžujú infekciu.
Stavba a genetika fágov
Typická stavba niektorých komplexnejších fágov (napríklad tailed bacteriophages) obsahuje hlavičku (kapsidu) s genetickým materiálom, chvostové štruktúry slúžiace na prichytenie a prenos DNA/RNA do hostiteľskej bunky a niekedy aj špecifické proteíny, ktoré degradujú bakteriálnu stenu. Jednoduchšie fágové častice môžu byť len kapsidou obklopujúcou nukleovú kyselinu.
Genómy fágov kódujú proteíny potrebné na replikáciu, štruktúrne bielkoviny kapsidy a často aj enzymatické faktory (napr. depolymerázy, endolysíny), ktoré štiepia bakteriálnu stenu alebo extracelulárne matrix biofilmov. Niektoré gény môžu niesť aj faktory ovplyvňujúce virulenciu baktérií – to má význam pri horizontálnom prenose génov.
Životný cyklus: lytický vs. lyzogénny
- Lytický cyklus – fág napadne baktériu, replikuje sa v nej, skladá nové virióny a nakoniec bunka praskne (lyzuje), uvoľní sa veľké množstvo nových fágoch schopných infikovať ďalšie baktérie.
- Lyzogénny (temperentný) cyklus – fág integruje svoj genóm do bakteriálneho chromozómu alebo zostáva ako profág v bunke, kde sa replikuje spolu s bakteriálnou DNA bez okamžitého zničenia hostiteľa. Profág môže neskôr prejsť do lytickej fázy.
Tieto dve stratégie majú rôzne dôsledky pre ekológiu mikroorganizmov a pre využitie fágov v terapii — pre liečbu infekcií sa zvyčajne preferujú striktne lytické fágy, pretože pri nich nedochádza k prenosu génov hostiteľa.
Výskyt a ekologická úloha
Fágy regulujú baktériálne populácie a ovplyvňujú tok genetickej informácie v mikrobiálnych spoločenstvách prostredníctvom transdukcie (prenášanie baktériálnych génov medzi bunkami). V morských ekosystémoch prispievajú k uvoľňovaniu organickej hmoty z lyzovaných buniek, čím ovplyvňujú biogeochemické cykly. V črevách a pôde pôsobia na skladby mikrobioty a môžu mať vplyv na zdravie hostiteľa.
Fágová terapia a liečba rezistentných baktérií
Fágová terapia využíva baktériofágy na cielené ničenie patogénnych baktérií. Výhody:
- vysoká špecificita voči cieľovým baktériám, takže menej poškodzujú prospešnú mikroflóru;
- schopnosť evolučne sa prispôsobovať spoločnému vývoju s baktériami;
- možnosť použiť fágové koktaily (kombinácie rôznych fágov) na zníženie rizika vzniku rezistencie;
- využitie fágových enzýmov (napr. endolysínov) ako antimikrobiálnych látok, často s rýchlym účinkom na gram-pozitívne baktérie.
Historicky sa fágová terapia rozvíjala predovšetkým v krajinách bývalého Sovietského zväzu (napríklad v Eliava Institute v Tbilisi) a v Poľsku; v západnej medicíne sa využívanie obnovilo najmä v posledných dekádach v dôsledku rastúcej rezistencie na antibiotiká. V posledných rokoch pribúdajú klinické štúdie a príbehy o tzv. compassionate use prípadoch, kde fágy zachránili pacientov s multirezistentnými infekciami, hoci rozsiahle randomizované štúdie sú stále v priebehu.
Výzvy, obmedzenia a bezpečnosť
- fágová špecificita znamená, že pre liečbu je často nutné presné určenie patogéna a testovanie citlivosti na konkrétne fágy;
- možnosť vzniku fágovej rezistencie u baktérií — tak ako pri antibiotikách, aj tu prebieha evolučný súboj; časté riešenie sú koktaily a kombinácie s antibiotikami;
- riziko transdukcie nežiaducich génov (napr. génov rezistencie alebo virulencie) pri využívaní temperentných fágov — preto sa v terapii preferujú lytické fágy alebo geneticky upravené varianty;
- regulačné a výrobnotechnické prekážky — štandardizácia, bezpečnostné testy, výrobné postupy a schvaľovanie liekov sú náročné a líšia sa medzi krajinami;
- imunitná odpoveď hostiteľa môže znižovať účinnosť systémovo podaných fágov pri opakovaných podaniach.
Interakcia s biofilmami
Biofilmy sú spoločné bunkové spoločenstvá obklopené extracelulárnou matrix, ktoré často odolávajú antibiotikám. Niektoré fágy produkujú depolymerázy, ktoré rozkladajú matrix a umožňujú fágom (a často aj antibiotikám) preniknúť dovnútra. Na druhej strane existujú situácie, kde prítomnosť určitých fágov alebo profágov mení správanie baktérií a môže nepriamo podporovať pretrvávanie biofilmu. Preto sú účinné stratégie kombinované — fágové koktaily, fágové enzýmy alebo kombinácia s antibiotikami či mechanickými postupmi.
Aplikácie mimo medicíny
- potravinárstvo: kontrola patogénov na povrchoch a v potravinách (Salmonella, Listeria),
- poľnohospodárstvo: ošetrovanie rastlinných bakteriálnych chorôb a ochrana zvierat,
- biotechnológie a diagnostika: fágami založené biosenzory a detekčné systémy,
- sanitácia a kontrola biofilmov v priemyselných zariadeniach.
Izolácia, charakterizácia a inžinierstvo fágov
Fágy sa izolujú z prostredia (voda, pôda, fekálie) pomocou konkrétnych hostiteľských baktérií a metód ako plaque assay. Následne sa vykonáva genomické sekvenovanie, morfologická analýza (elektrónová mikroskopia) a testy bezpečnosti a účinnosti. Moderné prístupy zahŕňajú genetickú modifikáciu fágov na zvýšenie ich lytickej aktivity, rozšírenie hostiteľského spektra alebo odstránenie nežiaducich génov. CRISPR a iné molekulárne nástroje umožňujú precíznejšie úpravy.
Perspektívy a výskum
Výskum fágov pokračuje v oblastiach: lepšie pochopenie interakcií s imunitným systémom hostiteľa, vývoj stabilných fabrikátov a formulácií pre klinické použitie, ďalšie klinické štúdie potvrdzujúce účinnosť a bezpečnosť a rozvoj fágových produktov pre priemyselné aplikácie. Kombinované prístupy (fágy + antibiotiká, fágové enzýmy, nanotechnológie) poskytujú sľubné stratégie v boji proti multirezistentným bakteriálnym infekciám.
Zhrnutie
Bakteriofágy sú všadeprítomné vírusy baktérií s rozmanitou stavbou a životnými stratégiami. Majú významné ekologické funkcie a veľký potenciál v medicíne ako alternatíva alebo doplnok k antibiotikám, najmä pri liečbe multirezistentných infekcií. Ich využitie prináša výhody, ale tiež výzvy, ktoré si vyžadujú ďalší výskum a starostlivú reguláciu.