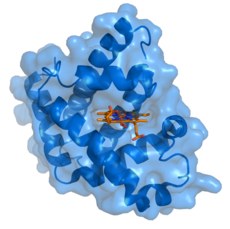
Ligand je biochemická látka, ktorej úlohou je viazať sa na biologickú molekulu (často na proteín) a vyvolať alebo modulovať určitú funkciu. Väzba ligandu mení konformáciu receptorového proteínu a tým ovplyvňuje jeho aktivitu, lokalizáciu alebo interakcie s ďalšími molekulami. Ligand môže pôsobiť ako spúšťač signálu, blokátor alebo kofaktor v rôznych biologických procesoch.
Mechanizmus väzby
V užšom zmysle ide o molekulu spúšťajúcu signál, ktorá sa viaže na miesto na cieľovom proteíne. K väzbe dochádza prostredníctvom rôznych medzimolekulových síl, medzi ktoré patria iónové väzby, vodíkové väzby, van der Waalsove sily a hydrofóbne interakcie. Súbor týchto síl určuje špecificitu a silu väzby. Dokovanie (asociácia) je zvyčajne reverzibilné (disociácia), hoci niektoré ligandy tvoria kovalentné väzby a viažu sa nereverzibilne.
Typy ligandov
- Endogénne signálne molekuly: hormóny (napr. inzulín), neurotransmitery (napr. acetylcholín, dopamín), rastové faktory.
- Substráty a produkty enzýmov: substráty sú ligandy enzýmov, pričom väzba často vedie k chemickej premene.
- Modulátory a liečivá: inhibítory (kompetitívne alebo nekompetitívne), aktivátory, agonisty, antagonisty, či čiastoční agonisti.
- Koenzýmy a kofaktory: malé molekuly alebo ióny potrebné pre katalytickú aktivitu (napr. NAD+, metalické ióny).
- Exogénne toxíny a lieky: molekuly z prostredia, ktoré sa viažu na proteíny a menia ich funkciu.
Afinitа, účinnosť a kinetika
Tendencia alebo sila väzby sa nazýva afinita. Afinitu možno kvantifikovať pomocou disociačnej konštanty (KD): nižšie KD znamená vysokú afinitu. Okrem afinity je dôležitá aj kinetika väzby — rýchlostné konštanty asociácie (kon) a disociácie (koff) určujú, ako rýchlo sa ligand viaže a uvoľní. Eficacia (účinnosť) popisuje, do akej miery ligand po viazaní aktivuje alebo inhibuje funkciu proteínu.
Režimy interakcie
- Agonista — viaže sa a aktivuje receptor.
- Antagonista — viaže sa, ale nevyvoláva aktiváciu; blokuje účinok agonistu.
- Čiastočný agonista — aktivuje receptor len čiastočne, aj pri saturácii.
- Inverzný agonista — znižuje konstitutívnu (základnú) aktivitu receptora.
- Allosterický modulátor — viaže sa na iné miesto než aktívne centrum a moduluje odpoveď pri viazaní ligandu (pozitívne alebo negatívne).
- Kompetitívna vs. nekompetitívna inhibícia — kompetitívne ligandy súperia o rovnaké väzbové miesto; nekompetitívne sa viažu inde a menia funkciu nezávisle od súťaženia.
Príklady a biologický význam
Medzi ligandy patria okrem iného substráty, inhibítory, aktivátory a neurotransmitery. Ligandy riadia signalizáciu medzi bunkami, regulujú metabolizmus, kontrolujú génovú expresiu a zúčastňujú sa na imunitných reakciách. Napríklad neurotransmitery prenášajú nervové signály cez synapsy, hormóny koordinujú endokrinné odpovede a lieky cielené na špecifické receptory menia priebeh chorôb.
Štúdium väzieb ligand–receptor
Affinity a interakcie ligand–receptor sa skúmajú viacerými metódami:
- Radioligandové viazanie — kvantifikácia špecifickej väzby pomocou značených ligandov.
- Surface plasmon resonance (SPR) — meranie kinetiky v reálnom čase.
- Isothermal titration calorimetry (ITC) — priame meranie termodynamiky väzby.
- Röntgenová kryštalografia a kryo-EM — určovanie štruktúry komplexu ligand–protein.
- Biochemické a buněčné assay — hodnotenie funkčných účinkov väzby (enzýmová aktivita, signalizácia, odpoveď bunky).
Význam v liečbe a výskume
Ligandy sú kľúčové v návrhu liekov: identifikácia a optimalizácia ligandov s vysokou afinitou a vhodnou účinnosťou je základom farmaceutického vývoja. Porozumenie mechanizmu väzby pomáha znižovať nežiadúce účinky, zvyšovať selektivitu a vytvárať nové terapeutické stratégie, vrátane modulátorov allosterických miest či cieľania špecifických izoforiem receptorov.
V skratke, ligand je univerzálna kategória molekúl, ktoré interagujú s biologickými makromolekulami a zásadne ovplyvňujú ich funkciu — od bežných metabolických reakcií až po komplexnú bunkovú signalizáciu a farmakologické zásahy.