Röntgenová kryštalografia je metóda, ktorá umožňuje určiť presné trojrozmerné usporiadanie atómov v molekulách a chemických zlúčeninách. Pri meraní sa na vzorku vysielajú röntgenové lúče a ich interakcia s elektrónovým mračnom atómov spôsobí rozptyl žiarenia. Tento rozptyl vytvára difrakčný vzor — súbor bodov a prúžkov — ktorý sa zaznamená na detektor. Z nameraného vzoru sa pomocou matematických metód (Fourierovej transformácie a ďalšej analýzy) rekonštruuje obraz hustoty elektrónov v kryštáli a z neho sa zostaví presný atómový model molekuly. Technika sa dá použiť pre organické aj anorganické látky; pri správnom postupe vzorka zvyčajne nie je spotrebovaná, hoci môže trpieť radiačným poškodením, najmä u biologických kryštálov.
Túto techniku vynašli spoločne sir William Bragg (1862-1942) a jeho syn sir Lawrence Bragg (1890-1971). V roku 1915 získali Nobelovu cenu za fyziku. Lawrence Bragg je najmladším laureátom Nobelovej ceny. Bol riaditeľom Cavendishovho laboratória na Cambridgeskej univerzite, keď vo februári 1953 James D. Watson, Francis Crick, Maurice Wilkins a Rosalind Franklinová objavili štruktúru DNA.
Ako to funguje (zjednodušene)
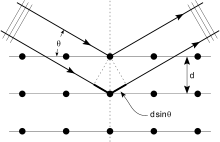
Röntgenové lúče majú vlnovú dĺžku porovnateľnú s medzikruhovými vzdialenosťami v kryštáloch (rádovo angström = 10⁻¹⁰ m). Lúče sa rozptyľujú na elektrónoch atómov a vlny sa navzájom interferujú. Výsledný difrakčný vzor nesie informácie o pravidelnom usporiadaní atómov. Základný vzťah popisujúci difrakciu je Braggov zákon: nλ = 2d sin θ, kde λ je vlnová dĺžka röntgenového žiarenia, d medziplánová vzdialenosť v kryštále, θ uhol dopadu a n celé číslo (poradie rozptylu). Tento zákon pomáha prepojiť pozície difrakčných špičiek so vzdialenosťami v kryštálovej mriežke.
Postup merania (krok za krokom)
- Príprava kryštálu: pre presnú analýzu je potrebný dobre usporiadaný kryštál. Pre malé molekuly sú kryštály relatívne ľahko dostupné, pre veľké biologické molekuly (proteíny) je často najnáročnejším krokom rast vhodných kryštálov.
- Zber difrakčných dát: kryštál sa umiestni do röntgenového difraktometra alebo na zdroj röntgenového žiarenia (laboratórny zdroj alebo synchrotrón). Otáčaním kryštálu sa sníma množstvo snímok z rôznych uhlov a na detektore sa zaznamenáva difrakčný vzor.
- Spracovanie dát: intenzity difrakčných špičiek sa indexujú, korigujú a normalizujú. Získané intenzity sa využívajú pri výpočte elektrónovej hustoty pomocou Fourierovej analýzy.
- Modelovanie a rafinácia: do mapy hustoty elektrónov sa vkladá atómový model (umiestnenie atómov a väzieb) a model sa opakovane rafinuje, aby čo najlepšie vysvetľoval namerané dáta. Hodnoty ako rozlíšenie (v Å) a R-faktor sa používajú na posúdenie kvality modelu.
- Interpretácia: finálny model poskytuje trojrozmernú polohu atómov, väzbové uhly, konformácie molekúl a často i polohy viazaných látok alebo iónov.
Výhody a obmedzenia
Výhody: veľmi vysoké priestorové rozlíšenie (až pod 1 Å pre malé molekuly), presné určenie polohy atómov, široké použitie od minerálov po proteíny a liečivá. Metóda je dobre overená a existuje množstvo softvéru a databáz (napr. PDB pre biologické štruktúry).
Obmedzenia: potrebný je kryštál — nie všetky molekuly sa dobre kryštalizujú. Biologické kryštály sú citlivé na radiačné poškodenie, preto sa často používajú kryokondície (ochladenie) alebo synchrotrónové zdroje s rýchlym zberom dát. Tiež existuje tzv. fázový problém (strata fázy pri meraní), ktorý treba riešiť metódami ako viacnásobné anomálne rozptylovanie (MAD/SAD), molekulárna náhrada alebo izomorfná substitúcia.
Aplikácie
- Určenie trojrozmerných štruktúr proteínov, nukleových kyselín a komplexov — kľúčové pre pochopenie funkcie a návrh liečív.
- Analýza malých organických a anorganických zlúčenín v chémii a materiálovom výskume.
- Identifikácia minerálnych fáz a štúdium kryštalografie pevných látok.
- Farmaceutický priemysel — kontrola polymorfizmu, určenie viažucich miest liečiv na cieľové molekuly.
Alternatívne a doplňujúce metódy
Pre prípady, keď kryštalizácia nie je možná, sa používajú iné techniky ako kryo-elektrónová mikroskopia (cryo-EM) alebo nukleárna magnetická rezonancia (NMR). Každá metóda má svoje silné a slabé stránky a často sa kombinujú, aby poskytli čo najúplnejší obraz o štruktúre a dynamike molekúl.
Röntgenová difrakcia zostáva jedným z najdôležitejších nástrojov vo vede o materiáloch, chémii a biologických vedách vďaka svojej schopnosti priamo zobrazovať atómové usporiadanie a tým odhaľovať súvislosti medzi štruktúrou a funkciou.