Atóm je základnou jednotkou hmoty. Je to najmenšia vec, ktorá môže mať chemickú vlastnosť. Existuje mnoho rôznych typov atómov, pričom každý má svoj vlastný názov, atómovú hmotnosť a veľkosť. Tieto rôzne atómy sa nazývajú chemické prvky. Chemické prvky sú usporiadané v periodickej tabuľke prvkov. Príkladmi prvkov sú vodík a zlato.
Atómy sú veľmi malé, ale ich presná veľkosť závisí od prvku. Šírka atómov sa pohybuje od 0,1 do 0,5 nanometra. Jeden nanometer je približne 100 000-krát menší ako šírka ľudského vlasu. To znemožňuje vidieť atómy bez špeciálnych nástrojov. Vedci používajú experimenty, aby zistili, ako fungujú a ako interagujú s inými atómami.
Atómy sa spájajú do molekúl: napríklad dva atómy vodíka a jeden atóm kyslíka sa spoja do molekuly vody. Keď sa atómy spoja, nazýva sa to chemická reakcia.
Atómy sa skladajú z troch druhov menších častíc, ktoré sa nazývajú protóny (majú kladný náboj), neutróny (nemajú náboj) a elektróny (majú záporný náboj). Protóny a neutróny sú ťažšie a zostávajú v strede atómu. Nazývajú sa jadro. Obklopuje ich oblak elektrónov, ktoré sú veľmi ľahké. Ku kladnému náboju jadra ich priťahuje elektromagnetická sila.
Počet protónov a elektrónov v atóme nám určuje, o aký prvok ide. Napríklad vodík má jeden protón a jeden elektrón; prvok síra má 16 protónov a 16 elektrónov. Počet protónov je atómové číslo. Okrem vodíka má jadro aj neutróny. Počet protónov a neutrónov spolu predstavuje atómovú hmotnosť.
V plynnom skupenstve sa atómy pohybujú rýchlejšie (pretože sa môžu voľne pohybovať) ako v kvapalnom skupenstve a v pevnej látke. V pevných látkach sú atómy tesne vedľa seba, takže vibrujú, ale nemôžu sa pohybovať (nemajú priestor) ako atómy v kvapalinách.
Štruktúra atómu — podrobnejšie
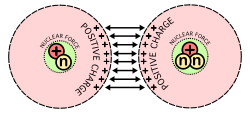
Atóm má dve základné časti: jadro a elektrónový obal. Jadro obsahuje protóny a neutróny a nesie takmer celú hmotnosť atómu. Protóny a neutróny majú hmotnosť približne 1 atómovej hmotnostnej jednotky (1 u) každá, kým elektróny sú približne 1 800-krát ľahšie. Jadro drží pokope silná nukleárna sila (tzv. silná interakcia), ktorá prevažuje nad odpudivou elektromagnetickou silou medzi kladne nabitými protónmi.
Elektróny sa neotáčajú po pevných dráhach, ako sa to kedysi predstavovalo; podľa kvantovej mechaniky sa nachádzajú v rozloženom elektrónovom oblaku tvorenom orbitálmi. Orbitál opisuje pravdepodobnosť, kde sa elektrón nachádza. Elektróny zaberajú určité energetické hladiny alebo vrstvy (shelly), a práve obsadenie týchto vrstiev ovplyvňuje chemické vlastnosti atómu.
Atómové číslo, izotopy a ióny
Atómové číslo (počet protónov) určuje identitu prvku. Dva atómy toho istého prvku majú rovnaký počet protónov, ale môžu sa líšiť v počte neutrónov — také varianty nazývame izotopy. Niektoré izotopy sú stabilné, iné sú nestabilné (radioaktívne) a rozpadávajú sa za vzniku žiarenia.
Ak atóm stratí alebo získa elektróny, stáva sa iónom: stratou elektrónu vzniká kladne nabitý kation, získaním elektrónu záporne nabitý anion. Ióny hrajú kľúčovú rolu v elektrochemií, biologických procesoch a v rôznych materiálových vlastnostiach.
Elektrónová konfigurácia a chemické väzby
Elektrónová konfigurácia (rozloženie elektrónov do vrstiev a orbitalov) rozhoduje o tom, ako sa atóm správa v chemických reakciách. Elektróny v vonkajšej vrstve — tzv. valenčné elektróny — určujú schopnosť tvoriť väzby. Najdôležitejšie typy väzieb sú:
- kovalentná väzba – zdieľanie páru elektrónov medzi atómami (napr. vo vode),
- iónová väzba – elektrostatické priťahovanie medzi iónmi s opačným nábojom (napr. v kuchynskej soli),
- metalická väzba – delokalizované elektróny v kovoch, ktoré umožňujú vodivosť,
- slabšie interakcie ako vodíkové mostíky a van der Waalsove sily, ktoré tiež ovplyvňujú vlastnosti látok.
Veľkosť atómov a ako ich pozorujeme
Ako už bolo uvedené, typické rozmery atómov sú rádovo 0,1–0,5 nanometra. Pri presnej definícii sa používa viac veličín — kovalentný polomer, van der Waalsov polomer alebo iontový rádius — podľa spôsobu merania a chemického prostredia.
Priame „fotografovanie“ atómov nie je možné klasickým mikroskopom, no moderné prístroje umožňujú zobraziť a manipulovať s jednotlivými atómami:
- skúsenosti s skanovacím tunelovým mikroskopom (STM) a atómovo-sílnym mikroskopom (AFM),
- transmísna elektronová mikroskopia (TEM) pre štruktúrne informácie,
- spektrálne metódy (napr. absorpčná a emisná spektrometria) poskytujú informácie o energiách a zložení atómov.
Atómy v rôznych skupenstvách látky
V plynnom skupenstve majú atómy alebo molekuly veľkú voľnosť pohybu a vysokú kinetickú energiu. V kvapalinách sú častice bližšie pri sebe a môžu sa posúvať, čo umožňuje tok a difúziu. V pevnom skupenstve sú atómy pevne usporiadané do mriežok (v kryštáloch) alebo neusporiadané (v amorfných látkach), pričom ich pohyb je obmedzený na kmitanie okolo rovnovážnych polôh.
Význam atómov v prírode a technológii
Atómy a ich kombinácie tvoria všetko okolo nás — od vzduchu a vody až po zložité biologické molekuly a materiály používané v priemysle. Poznanie atómovej štruktúry umožnilo rozvoj chemických syntéz, moderných materiálov, elektroniky, medicíny (napr. rádioaktívne izotopy v diagnostike a liečbe) a jadrovej energie.
Stručné zhrnutie
Atóm je základná stavebná jednotka hmoty, zložená z jadra (protóny a neutróny) a obalu elektrónov. Jeho vlastnosti (atómové číslo, izotopy, elektrónová konfigurácia) rozhodujú o chemickom správaní a o mieste v periodickej tabuľke. Moderná veda pomocou prístrojov a teórií kvantovej mechaniky dokáže popísať a využiť správanie atómov v rôznych oblastiach každodenného života a techniky.