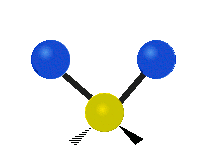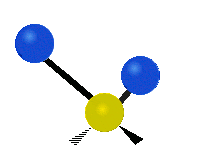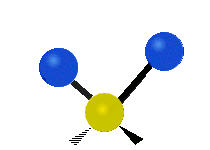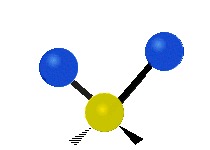
Molekulové vibrácie sú jedným z troch základných druhov pohybu molekúl, spolu s translačným pohybom (keď sa celá molekula pohybuje tým istým smerom) a rotačným pohybom (keď sa molekula rotuje okolo nejakej osi). Tieto vibrácie vznikajú, keď sa menia vzdialenosti a uhle medzi atómami v molekule; model „guličky spojené pružinou“ (harmonický oscilátor) dobre ilustruje základný charakter takéhoto pohybu.
Základné pojmy
Vibrácia je periodický pohyb atómov okolo rovnovážnych polôh. V najjednoduchšom (harmonickom) priblížení sú tieto pohyby opísané ako kmitanie s určitou frekvenciou a energiou. Skutočné molekuly však vykazujú anharmonické správanie — to znamená, že frekvencie a energetické stupne nie sú presne pravidelné a objavujú sa overtóny alebo kombinované pásy.
Typy vibračných pohybov
- Strečing (naťahovanie) – zmena dĺžky väzby medzi dvoma atómami. Môže byť symetrické (všetky väzby sa natiahnu/zoskrátia súčasne) alebo asymetrické (jedna väzba sa natiahne, zatiaľ čo druhá sa skráti).
- Bending (ohybové) – zmena uholov medzi väzbami, napr. scissoring (nožnice), rocking (hojdanie), wagging (kývanie) alebo twisting (krútenie).
- Torsionálne módy – krútenie častí molekuly okolo väzby (časté pri väčších organických molekulách).
Počet vibračných módov
Počet nezávislých (normálnych) vibračných módov závisí od počtu atómov N v molekule a od toho, či je molekula lineárna alebo nelineárna:
- Lineárna molekula: 3N − 5 vibračných módov
- Nelineárna molekula: 3N − 6 vibračných módov
Napríklad pre diatomickú molekulu (N = 2) je 3·2 − 5 = 1 — existuje teda len jeden vibračný mód: strečing väzby (naťahovanie/zoskupovanie).
Príklady: vodík H2, dusík N2, kyslík O2
Diatomické molekuly ako vodík H2, dusík N2 a kyslík O2 majú iba jeden vibračný mód — longitudinálne „naťahovanie“/„stláčanie“ väzby medzi dvoma atómami. V dôsledku toho sú ich vibračné spektrá relatívne jednoduché.
Avšak všetky tri sú homonukleárne diatomy (atóm + ten istý atóm), takže pri ideálnom modeli sa ich vibrácie nemenia elektrostatický dipól molekuly — preto sú tieto vibrácie IR-inaktívne (neradia sa do infračerveného spektra podľa dipólových selekčných pravidiel). Naopak, zmeny polarizovateľnosti pri vibrácii môžu viesť k tomu, že tieto módy sú Raman-aktívne, takže sú pozorovateľné v Ramanovej spektroskopii.
Ľahšie molekuly (ako H2) majú vyššie vibračné frekvencie než ťažšie (N2, O2) pri podobnej sile väzby — to je dôsledok závislosti frekvencie na redukovanej hmote sústavy v harmonickom oscilátore.
Spektroskopia a praktické dôsledky
Vibrácie sa študujú najčastejšie pomocou infračervenej (IR) spektroskopie a Ramanovej spektroskopie. Výber metódy závisí na tom, či vibrácia mení dipólový moment (IR) alebo polarizovateľnosť molekuly (Raman). Pre komplexnejšie molekuly poskytuje analýza vibračných módov informácie o väzbových konštantách, geometrii molekuly a medziľudských interakciách (napr. vodíkové väzby).
Dodatočné poznámky
Vibrácie sú kľúčové nielen pre základnú fyziku a chémiu, ale aj pre aplikácie v materiálových vedách, analytickej chémii (identifikácia látok), astrochemii (identifikácia molekúl v medzihviezdnom priestore) a v spektroskopii prostredia. Pri praktickom skúmaní treba brať do úvahy aj faktory ako anharmonicita, teplotný rozptyl, tlmenie a interakcie s okolím, ktoré môžu posunúť alebo rozšíriť vibračné pásy.