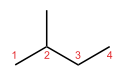Štruktúrna (konštitučná) izoméria — definícia, typy a príklady
Štruktúrna (konštitučná) izoméria: definícia, typy (skeletové, polohové/regio-, funkčné/tautoméry) a príklady s jasným vysvetlením pre študentov a chemikov.
Štruktúrna izoméria (IUPAC ju nazýva konštitučná izoméria) je druh izomérie, pri ktorej majú dve (alebo viac) látok rovnaký molekulový vzorec, ale atómy sú v molekulách naviazané v inom poradí. Inak povedané, izoméry sa líšia vzájomným usporiadaním väzieb medzi atómami, čo vedie k odlišným chemickým a fyzikálnym vlastnostiam. Opakom štruktúrnej izomérie je stereoizoméria, pri ktorej je poradie väzieb rovnaké, mení sa však priestorové usporiadanie atómov.
Typy konštitučnej (štruktúrnej) izomérie
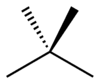
- Skeletová (reťazová) izoméria – líši sa usporiadanie uhlíkového reťazca (lineárny vs rozvetvený). Príklad: n-bután (CH3–CH2–CH2–CH3) a izobután (2‑metylproprán, (CH3)2CH–CH3) majú rovnaký vzorec C4H10, ale rôznu štruktúru a rozdielne fyzikálne vlastnosti (napr. bod varu: n‑bután ≈ −0,5 °C, izobután ≈ −11,7 °C).
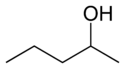
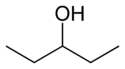
- Polohová (pozičná, regio) izoméria – rovnaký kostrový rámec, ale funkčná skupina alebo viaceré substituenty sú v rôznych pozíciách. Príklady: 1‑propanol vs 2‑propanol (C3H8O), alebo orto/meta/para‑xylény (rozdielne polohy metylových skupín na benzénovom kruhu).
- Funkčná izoméria – izoméry majú rozdielne funkčné skupiny napriek rovnakému molekulovému vzorcu. Klasický príklad: etanol (CH3CH2OH) a dimetyléter (CH3OCH3), oba C2H6O, ale s veľmi odlišnými vlastnosťami (etanol je kvapalina s bodom varu ≈ 78 °C; dimetyléter je pri normálnych podmienkach plyn, bp ≈ −24 °C).
- Tautomeria – špeciálny typ funkčnej izomérie, pri ktorej sa izoméry (tautoméry) rýchlo navzájom premieňajú prostredníctvom presunu protónu a zmeny polohy mnohonásobnej väzby. Najčastejší prípad je keto‑enol tautomeria (napr. u acetylacetónu je významná prítomnosť enolovej formy stabilizovanej intramolekulárnym vodíkovým väzbou).
- Ring‑chain (cyklo‑reťazová) izoméria – rovnaký vzorec môže tvoriť otvorený reťazec alebo cyklický derivát. Napríklad niektoré alkény (pentén) a cykloalkány (cyklopentán) môžu mať rovnaký sumárny vzorec (C5H10) a predstavujú ring‑chain izoméry.
- Metameria – historicky používaný pojem pre izomériu látok obsahujúcich heteroatóm, kde sa mení zloženie alkylových zvyškov okolo heteroatómu (napr. rôzne étery so sumárnym vzorcom C4H10O: dietyléter vs metyl‑propyléter).
Vplyv na vlastnosti a praktický význam
Konštitučné izoméry majú zvyčajne rozdielne fyzikálne (bod varu, bod topenia, rozpustnosť, hustota) aj chemické vlastnosti (reaktivita, kyslosť/zásaditosť, schopnosť tvoriť vodíkové väzby). Preto je identifikácia a kontrola izomérneho zloženia dôležitá v syntéze organických látok, farmaceutikách, petrochemickom priemysle a pri vývoji materiálov.
Analytické rozlíšenie izomérov
- Spektroskopia: 1H a 13C NMR (detailné informácie o prostredí atómov vodíka a uhlíka), IR (funkčné skupiny), UV/VIS (konjugované systémy).
- Hmotnostná spektrometria (MS) – fragmentačné vzory môžu pomôcť rozlíšiť typy izomérov.
- Chromatografické metódy (GC, HPLC) – separujú izoméry podľa polarity, veľkosti a interakcií s fázou.
- Fyzikálne merania – bod varu, bod topenia, hustota a rozpustnosť často významne líšia štruktúrne izoméry.
Krátke zhrnutie
Štruktúrna (konštitučná) izoméria zahŕňa súbor typov izomérie, pri ktorých sa mení usporiadanie väzieb v molekule pri zachovaní sumárneho vzorca. Medzi hlavné typy patria skeletová, polohová, funkčná (vrátane tautomérie), ring‑chain a metameria. Rozlíšenie izomérov je kľúčové pre pochopenie ich chemického správania a pre aplikácie v priemysle a výskume.
Skeletálna izoméria
Pri izomerii skeletu alebo izomerii reťazca sa zložky skeletu (zvyčajne uhlík) preskupujú tak, aby vytvárali rôzne štruktúry. Pentán má tri izoméry. Sú to n-pentán (často nazývaný jednoducho "pentán"), izopentán (metylbután) a neopentán (dimetylpropán).
| Skeletová izoméria pentánu | ||
|
|
|
|
| n-pentán | Izopentán | Neopentán |
Izomeria polohy
Pri polohovej izomérii funkčná skupina alebo iný substituent mení svoju polohu v základnej štruktúre. V nasledujúcej tabuľke sa hydroxylová skupina môže nachádzať v troch rôznych polohách na n-pentánovom reťazci a vytvoriť tri rôzne zlúčeniny.
| Príklad polohovej izomerie | ||
|
|
|
|
| 1-pentanol | 2-pentanol | 3-pentanol |
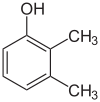
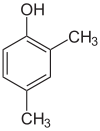
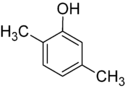
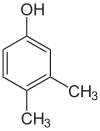
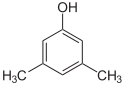
Existuje mnoho aromatických izomérov, pretože substituenty môžu byť umiestnené na rôznych častiach benzénového kruhu. Existuje len jeden izomér fenolu alebo hydroxybenzénu, ale krezol alebo metylfenol má tri izoméry, v ktorých môže byť prídavná metylová skupina umiestnená na troch rôznych miestach kruhu. Xylénol má jednu hydroxylovú skupinu a dve metylové skupiny a celkovo existuje 6 izomérov.
| Pozičné izoméry xylénu | ||
|
|
|
|
| 2,3-xylénol | 2,4-xylénol | 2,5 xylénol |
|
|
|
|
| 2,6-xylénol | 3,4-xylénol | 3,5-xylenol |
Izomerizácia funkčných skupín
Funkčné izoméry sú jedným zo štrukturálnych izomérov. Dve zlúčeniny vo funkčnej izomérii majú rovnaký molekulový vzorec (číslo každého atómu je rovnaké, napríklad cyklohexán:C
6H
12 a 1-hexén:C
6H
12). Ale atómy sú spojené iným spôsobom, takže ich skupenstvo je odlišné. Tieto skupiny atómov nazývame funkčné skupiny, funkčné skupiny alebo moety. Iný spôsob, ako to povedať, je, že dve zlúčeniny, ktoré majú rovnaký molekulový vzorec, ale majú rôzne funkčné skupiny, sú funkčné izoméry.
Napríklad chemický vzorec cyklohexánu a 1-hexénu je C6 H12 . Nazývame ich izoméry funkčnej skupiny, pretože cyklohexán je cykloalkán a hex-1-én je alkén.
| Príklad izomerie funkčných skupín | |
|
|
|
| 1-hexén | |
Aby boli dve molekuly funkčnými izomérmi, musia obsahovať kľúčové skupiny atómov usporiadané určitým spôsobom. Niektoré z najlepších príkladov pochádzajú z organickej chémie. C2 H6 O je molekulový vzorec. V závislosti od spôsobu usporiadania atómov môže predstavovať dve rôzne zlúčeniny dimetyléter CH3 -O-CH3 alebo etanol CH3 CH2 -O-H. Dimetyléter a etanol sú funkčné izoméry. Prvý je éter. Funkčný reťazec uhlík - kyslík - uhlíkový reťazec sa nazýva éter. Druhý je alkohol. Funkcia uhlíkový reťazec - kyslík - vodík sa nazýva alkohol.
Ak funkčné vlastnosti zostávajú rovnaké, ale ich umiestnenie sa mení, štrukturálne izoméry nie sú funkčnými izomérmi. 1-propanol a 2-propanol sú štrukturálne izoméry, ale nie sú funkčné izoméry. Oba sú alkoholy. Funkčná skupina (uhlíkový reťazec O-H) je prítomná v oboch týchto zlúčeninách, ale nie sú rovnaké.
Hoci niektorí chemici používajú pojmy štrukturálny izomér a funkčný izomér zameniteľne, nie všetky štrukturálne izoméry sú funkčné izoméry.
Funkčné izoméry sa v chémii najčastejšie identifikujú pomocou infračervenej spektroskopie. Infračervené žiarenie zodpovedá energiám spojeným predovšetkým s molekulovými vibráciami. Funkcionalita alkoholu má veľmi výraznú vibráciu nazývanú OH-stretch, ktorá je spôsobená vodíkovou väzbou. Všetky alkoholy v kvapalnom a pevnom skupenstve absorbujú infračervené žiarenie pri určitých vlnových dĺžkach.
Všetky zlúčeniny s rovnakými funkčnými skupinami budú absorbovať určité vlnové dĺžky infračerveného svetla, pretože s týmito skupinami sú spojené vibrácie. Infračervené spektrum sa v skutočnosti delí na dve oblasti. Prvá časť sa nazýva oblasť funkčných skupín. Dimetyléter a etanol by mali rozdielne infračervené spektrá v oblasti funkčných skupín.
Druhá časť infračerveného spektra sa nazýva oblasť odtlačkov prstov; súvisí s typmi pohybu, ktoré umožňuje symetria molekuly a ktoré ovplyvňujú energie väzieb. Oblasť odtlačkov prstov je špecifickejšia pre jednotlivé zlúčeniny. Hoci 1-propanol a 2-propanol majú podobné infračervené spektrá v oblasti funkčných skupín, v oblasti odtlačkov prstov sa líšia.
Zjednodušene povedané, funkčné izoméry sú štruktúrne izoméry, ktoré majú rôzne funkčné skupiny, napríklad alkohol a éter.
Počítanie izomérov
Ako príklad počtu izomérov možno uviesť 7 štruktúrnych izomérov s molekulovým vzorcom C3 H6 O, z ktorých každý má inú väzbovú spojitosť a je stabilný na vzduchu pri teplote okolia. Ďalšie dva štruktúrne izoméry sú enolové tautoméry karbonylových izomérov, ktoré však nie sú stabilné.
| Molekulárna štruktúra | Bod topenia (°C) | Bod varu (°C) | Komentár | |
| Allylalkohol |
| -129 | 97 | |
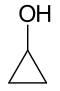
| Cyklopropanol |
| 101-102 | ||
| Propanal |
| - 81 | 48 | Tautomerický s (E)-1-propenolom a (Z)-1-propenolom |
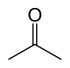
| Acetón |
| - 94.9 | 56.53 | Tautomerický s 2-propenolom |
| Oxetan |
| - 97 | 48 | |
| Oxid propylénový |
| - 112 | 34 | Možno rozlíšiť na dva enantioméry |
| Metylvinyléter |
| - 122 | 6 |
Prehľadať