Tento článok sa zaoberá len chemickými vlastnosťami alkoholov.
Alkohol používaný v nápojoch je etanol; viac informácií nájdete na stránke Alkoholické nápoje a alkoholizmus.
V chémii je alkohol všeobecný pojem, ktorý sa vzťahuje na mnohé organické zlúčeniny používané v priemysle a vede ako činidlá, rozpúšťadlá a palivá. Alkoholy nie sú sacharidy, ale sú tvorené alkylovou skupinou s jednou alebo viacerými hydroxylovými (-OH) skupinami viazanými na atómy uhlíka. Mnohé nízkomolekulárne alkoholy sú bezfarebné a tiež priehľadné, avšak nie všetky; vyššie alkoholy môžu byť voskovité alebo pevné a niektoré obsahujú farebné nečistoty.
Definícia a názvoslovie
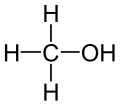
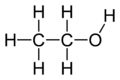
Alkoholy sú organické zlúčeniny obsahujúce jednu alebo viac hydroxylových skupín (-OH) viazaných na sp3-hybridizovaný atóm uhlíka. Podľa IUPAC sa názov alkoholov tvorí pridaním prípony „-ol“ k názvu uhlíkového reťazca (napr. metanol, etanol, propan-2-ol).
Klasifikácia
- Podľa počtu hydroxylových skupín: monooly (jedna -OH), dioly (dva -OH, napr. etylénglykol), trioly (napr. glycerol) a polyoly (mnoho -OH).
- Podľa typu uhlíkového atómu viazaného na -OH:
- primárne (R-CH2-OH),
- sekundárne (R-CH(OH)-R'),
- terciárne (R-C(OH)-R'-R'').
Fyzikálne vlastnosti
- Polárnosť a vodíkové väzby: Hydroxylová skupina je polárna a umožňuje vznik vodíkových väzieb medzi molekulami, čo zvyšuje body varu v porovnaní s nespárovanými uhľovodíkmi rovnakej hmotnosti.
- Rozpustnosť vo vode: Krátke reťazce (metanol, etanol) sú dobre rozpustné vo vode vďaka tvorbe vodíkových väzieb; rozpustnosť klesá so zvyšujúcou sa dĺžkou nepolárneho uhlíkového reťazca.
- Stav látky: Nižšie alkoholy sú zvyčajne kvapaliny; vyššie (s dlhými reťazcami) môžu byť vosky alebo pevné látky.
- Vzhľad a vôňa: Mnohé sú bezfarebné kvapaliny s charakteristickou vôňou, avšak vôňa a prítomnosť farby závisia od konkrétnej zlúčeniny a nečistôt.
Hlavné chemické reakcie alkoholov
- Oxidácia: Primárne alkoholy sa oxidujú na aldehydy a ďalej na karboxylové kyseliny; sekundárne na ketóny; terciárne sú voči bežnej oxidácii stabilné (vyžadujú silnejšie podmienky pre rozklad).
- Substitúcia (dehydratácia a halogenácia): Odvodnením (dehydratáciou) za prítomnosti silných kyselín vznikajú alkény. Reakciou s halogenovodíkmi vznikajú alkylhalogenidy.
- Esterifikácia: Reakciou s karboxylovými kyselinami (často katalyzovanou kyselinami) vznikajú estery a voda.
- Tvorba éterov: Williamsonova syntéza umožňuje tvorbu éterov z alkoxidov a alkylhalogenidov; kondenzáciou dvoch alkoholov (pri kyslom katalyzátore) vznikajú diétery.
- Tvorba alkoxidov: Reakciou s alkalickými kovmi (Na, K) sa tvoria alkoxidy (R-O−M+), ktoré sú silné nukleofily a zásady.
- Ďalšie reakcie: ochrana hydroxylovej skupiny (napr. silylácie), dehydrácie, transesterifikácie a ďalšie špecifické transformácie používané v organickej syntéze.
Príklady bežných alkoholov
- Metanol (CH3OH) – používaný ako rozpúšťadlo, palivo a v chemickej výrobe; veľmi toxický pri požití.
- Ethanol (etanol) – alkohol v nápojoch, rozpúšťadlo, palivo (bioetanol), antiseptikum.
- Propanol (n-propanol, izopropanol) – rozpúšťadlá a dezinfekčné prostriedky (isopropanol).
- Butanol – rôzne izoméry s priemyselnými aplikáciami a ako medziprodukt.
- Glycerol (glycerín) – triol používaný v kozmetike, potravinárstve a farmácii.
Použitie
- rozpúšťadlá v laboratóriách a priemysle,
- výroba plastov, liečiv, farbív a ďalších chemikálií,
- palivá a aditíva (metanol, etanol, butanol),
- antiseptiká a dezinfekčné prostriedky (isopropanol, ethanol),
- potravinárske a kozmetické prísady (glycerol, alkoholové extrakty).
Bezpečnosť a toxicita
- Alkoholy sú často horľavé a vyžadujú opatrné skladovanie a manipuláciu.
- Niektoré alkoholy (napr. metanol) sú vysoko toxické a môžu spôsobiť slepotu alebo smrť pri požití. Etanol je toxický pri vysokých dávkach a dlhodobej konzumácii (pozri odkazy na alkoholizmus a alkoholické nápoje).
- Pri práci s alkoholmi používajte vhodné ochranné prostriedky (rukavice, badateľné vetranie, protipožiarne opatrenia).
Pre hĺbkové informácie o biologických či sociálnych dôsledkoch konzumácie alkoholu alebo o konkrétnych aplikáciách jednotlivých alkoholov pozrite príbuzné články a odbornú literatúru.