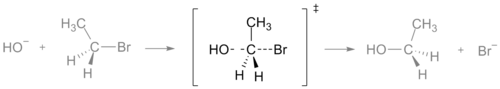Pri chemickej reakcii je prechodný stav bod na potenciálnej energii, v ktorom je energia reakčného systému maximálna. Táto energia sa nazýva aktivačná energia. Keď sa zmiešajú dve alebo viac molekúl, narazia do seba; ak majú pri náraze dostatočnú energiu a správnu orientáciu, prekonajú prechodný stav a premenia sa na produkty. V prechodnom stave sa čiastočne tvoria nové väzby a zároveň sa čiastočne rušia staré väzby — štruktúra je teda zvyčajne „medzi“ východzím a konečným stavom. V energetickom grafe sa prechodný stav často označuje symbolom dvojitej dýky ‡.
Rozdiel medzi prechodným stavom a medziproduktom
Je dôležité neplietať prechodné stavy s medziproduktmi. Prechodný stav leží v energetickom maxime a má extrémne krátku dobu života (typicky femtosekundy), pretože ide o nestabilnú konfiguráciu, ktorá okamžite pokračuje k produktom alebo späť k činidlám. Naopak medziprodukt sa nachádza v lokálnom energetickom minime a môže byť stabilný dostatočne dlho na to, aby sa dal izolovať alebo pozorovať priamo.
Energetický profil a aktivačná energia
Na energiou znázornenom profile reakcie sa zvyčajne rozlišujú:
- energia činidiel (východzí bod),
- energia prechodného stavu (vrchol) — od tejto hodnoty sa odvíja aktivačná energia,
- energia produktov (koncový bod).
Veľkosť aktivačnej energie určuje rýchlosť reakcie pri danej teplote: čím vyššia aktivačná energia, tým pomalšia reakcia bez katalýzy. V kinetike sa tento vzťah popisuje napríklad Arrheniovou rovnicou a teóriou prechodného stavu (Eyringova rovnica), ktoré spájajú rýchlostné konštanty s energickými parametrami.
Termodynamické a kinetyčné parametre prechodného stavu
Pri charakterizovaní prechodného stavu sa často uvádzajú:
- ΔG‡ — aktivačná Gibbsova energia (slúži na odhad rýchlosti reakcie),
- ΔH‡ — aktivačná entalpia (spojená s energetickými zmenami väzieb),
- ΔS‡ — aktivačná entropia (ovplyvňuje, či prechodný stav vyžaduje viac alebo menej usporiadania).
Tieto parametre sa dajú experimentálne odhadnúť z teplotnej závislosti rýchlostných konštánt a teoreticky vypočítať pomocou kvantovochemických metód.
Štruktúra prechodného stavu
Prechodný stav nie je pevnou molekulárnou „ličnosťou“, ale maxima na potenciálnej ploche; jeho geometria často obsahuje čiastočné väzby (naznačujúce súčasné tvorenie a lámanie väzieb). Príkladom je SN2 reakcia, kde prechodný stav vykazuje pentakoordinačnú uhlíkovú centrálnu časť s čiastočnými väzbami k nukleofílu aj odchádzajúcej skupine.
Ako sa prechodné stavy skúmajú
Priame skúmanie je náročné kvôli krátkej dobe života, ale existujú rôzne prístupy:
- experimentálne metódy: ultrarýchla (ultrafast) spektroskopia (femtosekundová), meranie kinetických izotopových efektov, použitie prechodnových stavovych analógov a kinetické štúdie, ktoré poskytujú nepriamy dôkaz o geometrii a energetike,
- teoretické a výpočtové metódy: kvantovochemické výpočty (DFT, ab initio), metódy na hľadanie prechodných stavov (napr. nudged elastic band, intrinsic reaction coordinate — IRC), ktoré predpovedajú geometriu a energetiku prechodného stavu,
- kombinované prístupy: porovnanie experimentálnych dát (rýchlosti, izotopových efektov, termodynamických parametrov) s výpočtmi pre získanie overenej štrukturálnej a energetickej interpretácie.
Význam v katalýze a biochemii
Katalyzátory fungujú tak, že znižujú aktivačnú energiu, často stabilizovaním prechodného stavu relatívnejšie viac než činidiel. Enzymy sú extrémne efektívne v tom, že viažu a stabilizujú prechodný stav — preto vznikajú účinné inhibítory ako prechodnové stavové analógy, ktoré napodobňujú geometriu prechodného stavu a viažu sa k enzymu silno.
Praktické príklady
- SN2 substitúcia: jednorazový prechodný stav s čiastočnými väzbami k nukleofílu aj odchádzajúcej skupine (lineárny útok),
- pericyklické reakcie: symetrický prechodný stav, často opisovaný postulátom Hammonda pri analýze podobnosti medzi prechodným stavom a reakčnými štádiami,
- protonový alebo vodíkový prenos: prechodný stav so silne posunutým protónom medzi donorom a akceptorom — často veľmi krátka doba života, ale pozorovateľné pomocou ultrarýchlych metód.
Zhrnutie
Prechodný stav je kľúčový koncept pri pochopení reakčných mechanizmov a pri predpovedaní rýchlosti reakcií. Štúdium prechodných stavov, kombinujúce experiment a výpočty, je dôležitou súčasťou chemickej kinetiky a vývoja katalytických systémov, vrátane enzýmov a priemyselných katalyzátorov.