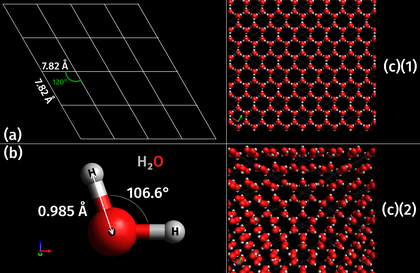
V kryštalografii je kryštálová štruktúra spôsob usporiadania atómov (alebo iónov či molekúl) v kryštalickom materiáli. Kryštály vznikajú prirodzene na základe spôsobu, akým sa spájajú chemické väzby atómov. V kryštáli sa vyskytujú symetrické opakujúce sa vzory v trojrozmernom priestore.
Kryštálová štruktúra a symetria spôsobujú mnohé fyzikálne vlastnosti, napríklad štiepnosť (spôsob štiepenia kryštálu), spôsob vedenia elektrického prúdu a optické vlastnosti.
Kryštálová štruktúra chemickej látky je tvar kryštálu na molekulovej úrovni. Existuje niekoľko tvarov kryštálov. Chlorid sodný je kocka. Síran meďnatý je triklinický. Väčšina vecí, dokonca aj kovov, má kryštálovú štruktúru. Do niektorých kryštálov sa zmestí viac atómov ako do iných a tieto kryštály zvyčajne vážia viac.
Základné pojmy
Jednotková bunka (unit cell) je najmenší opakujúci sa prvok kryštálovej mriežky, z ktorého sa skladá celý kryštál. Opakovaním jednotkovej bunky v priestore vzniká pravidelná mriežka atómov alebo iónov. Kryštálová mriežka (lattice) označuje súbor bodov, ktoré vyjadrujú pravidelné polohy atómov.
Koordinačné číslo udáva, koľko najbližších susedov má daný atóm v štruktúre (napr. v rock-salt štruktúre NaCl je koordinačné číslo 6, v FCC a HCP kovoch je 12).
Bravaisove mriežky a kryštalické sústavy
- V trojrozmernom priestore existuje 14 tzv. Bravaisových mriežok, ktoré sa ďalej zaraďujú do 7 kryštalických sústav: kubická, tetragonálna, ortorombická, monoklinická, triklinická, heksagonálna a trigónna (rhombohedrálna).
- Každá sústava má charakteristické tvary jednotkovej bunky a rôznu symetriu; kombinácia translácie a symetrických operácií dáva dokopy 230 možných priestorových skupín.
Bežné typy usporiadania
- Jednoducho kubická (SC) – nízka hustota balenia (~52 %), koordinačné číslo 6.
- Body-centered cubic (BCC) – napr. Fe pri izbovej teplote, vyššia pevnosť, koordinačné číslo 8.
- Face-centered cubic (FCC) – tzv. kubické plošne centrované, napr. Al, Cu, Ag; vysoká hustota balenia (~74 %), koordinačné číslo 12.
- Hexagonal close-packed (HCP) – ďalší typ tesného balenia (74 %), napr. Mg, Ti; koordinačné číslo 12.
Metódy určovania kryštálovej štruktúry
- Röntgenová difrakcia (XRD) – najčastejšia metóda; používa sa Braggov zákon na určenie vzdialeností medzi rovinami a symetrie.
- Elektrónová mikroskopia a difrakcia – umožňujú priestorové zobrazenie a analýzu na nanometrovej škále.
- Neutronová difrakcia – vhodná pri štúdiu polohy ľahkých prvkov (napr. vodík) a magnetických štruktúr.
Vplyv kryštálovej štruktúry na vlastnosti materiálov
Kryštálová štruktúra výrazne určuje makroskopické vlastnosti materiálov:
- Mechanické vlastnosti: pevnosť, tvárnosť a tvrdosť sú ovplyvnené dislokáciami, typom balenia (FCC sú vo všeobecnosti ťažšie deformovateľné plasticky než BCC pri nižších teplotách) a prítomnosťou šmykových rovin.
- Štiepnosť a lom: štruktúra a symetria určujú preferované roviny štiepenia (napr. diamant štiepi pozdĺž určitých rovín).
- Elektrické vlastnosti: vlnová funkcia elektrónov a pásová štruktúra závisia od periodického potenciálu – kovové vedenie, polovodičové a izolačné vlastnosti sú úzko späté s usporiadaním atómov.
- Optické vlastnosti: anisotropné kryštály môžu byť dvojlome (birefringentné), niektoré necentrosymetrické kryštály sú piezoelektrické alebo nelineárne optické.
- Tepelné vlastnosti: vodivosť tepla závisí na transporte fonónov a ich rozptylu na defektoch a mriežke.
- Hustota a balenie: efektívne balenie atómov (napr. FCC, HCP) vedie k vyššej hustote materiálu pri rovnakom chemickom zložení.
Defekty a anizotropia
Kryštály nie sú ideálne; existujú defekty, ktoré často určujú technologické vlastnosti:
- Point defekty: vakancie, intersticiálne atómy, substitučné atómy.
- Čiarové defekty: dislokácie, ktoré umožňujú plastickú deformáciu.
- Plošné defekty: hranice zŕn, vrstvy a skladania (twinning).
Tieto defekty ovplyvňujú mechanické správanie, elektrický odpor, koróziu a ďalšie vlastnosti materiálov.
Polymorfizmus a amorfnosť
Niektoré látky majú viacero kryštálových modifikácií (polymorfov) s rôznymi vlastnosťami — príkladom je uhlík: diamant (tetraédické väzby, veľmi tvrdý, izolačný) a grafit (vrstvená štruktúra, dobrý vodič v rovine vrstiev). Existujú aj amorfné (nekryštalické) materiály, ako sklo, ktoré nemajú dlhodobo pravidelnú mriežku a majú odlišné fyzikálne vlastnosti od kryštálov.
Použitie a význam
Pochopenie kryštálovej štruktúry je kľúčové v mnohých oblastiach: materiálové inžinierstvo (dizajn pevných zliatin), polovodičová technika (riadenie pásových štruktúr), farmaceutika (polymorfizmus ovplyvňuje rozpustnosť liečiva), geológia (určenie minerálov) a chemické syntézy.
Zhrnutie: Kryštálová štruktúra je základným faktorom, ktorý určuje vlastnosti materiálov. Poznanie typu mriežky, jednotkovej bunky, symetrie a defektov umožňuje predpovedať a cielene upravovať mechanické, elektrické, optické a tepelné správanie materiálov.