Teplo môže spôsobiť, že dvojité väzby vytvoria kruh. Tepelných cykloadícií sa zvyčajne zúčastňujú (4n + 2) π elektróny vo východiskovom materiáli pre určité celé číslo n. Z dôvodu orbitálnej symetrie je väčšina cykloadícií suprafaciálnych. Zriedkavo sú antarafaciálne-antarafaciálne. Existuje niekoľko príkladov tepelných cykloadícií, ktoré majú 4n π elektrónov (napríklad cykloadícia [2 + 2]). Tieto prebiehajú v suprafaciálnom-antarafaciálnom zmysle. Napríklad dimerizácia keténu má ortogonálny súbor p orbitálov. Tieto p orbitály umožňujú, aby reakcia prebiehala pomocou skríženého prechodového stavu.
Svetlo môže tiež spôsobiť, že dvojité väzby vytvoria kruh. V dôsledku fotochemickej aktivácie môže dôjsť aj k cykloadíciám, na ktorých sa zúčastňujú 4n π elektróny. V tomto prípade jedna zložka spôsobuje presun elektrónu z najvyššie obsadenej molekulovej orbitály (HOMO) (π väzba) do najnižšej neobsadenej molekulovej orbitály (LUMO) (π* antiväzba). Po postupe elektrónu do vyššieho orbitálu umožňuje orbitálna symetria, aby reakcia prebiehala nadväznostne. Príkladom je DeMayova reakcia. Ďalší príklad je uvedený nižšie, fotochemická dimerizácia kyseliny škoricovej.
Všimnite si, že nie všetky fotochemické (2+2) cyklizácie sú cykloadíciami; o niektorých je známe, že prebiehajú radikálovými mechanizmami.
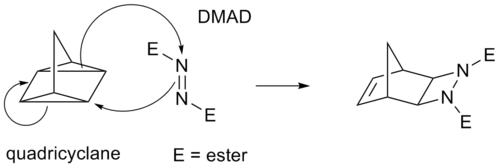
Niektoré cykloadície namiesto π väzieb prebiehajú cez napnuté cyklopropánové kruhy, ktoré majú výrazný π charakter. Napríklad analógom Dielsovej-Alderovej reakcie je reakcia kvadricyklán-DMAD:
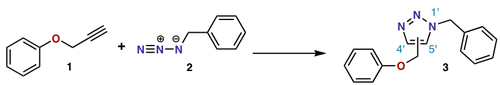
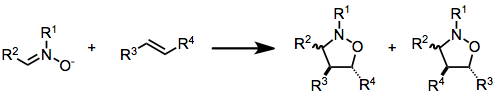
V zápise (i+j+...) cykloadície sa i a j vzťahujú na počet atómov zúčastnených na cykloadícii. V tomto zápise je Dielsova-Alderova reakcia (4+2)cykloadíciou a 1,3-dipolárna adícia, ako je prvý krok ozonolýzy, je (3+2)cykloadíciou. Tento zápis používa zátvorky. IUPAC však uprednostňuje zápis [i+j+...], ktorý počíta elektróny a nie atómy. Používa hranaté zátvorky. V tomto zápise sa Dielsova-Alderova reakcia a dipolárna reakcia stávajú [4+2]cykloadíciou. Reakcia medzi norbornadénom a aktivovaným alkynom je [2+2+2]cykloadícia.
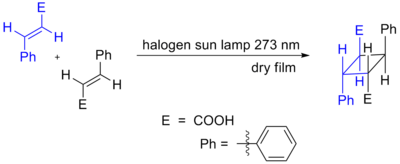
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)