Riadená evolúcia (DE) je experimentálna metóda proteínového inžinierstva, ktorá sa používa na vytváranie alebo optimalizáciu enzýmov a ďalších proteínov pre priemyselné, environmentálne alebo lekárske účely. Metóda napodobňuje proces prirodzeného výberu cez iteratívne mutovanie a selekciu, pričom cielom je získať varianty s požadovanými vlastnosťami (vyššia aktivita, stabilita pri vyššej teplote, odolnosť voči rozpúšťadlám, zmena špecificity a pod.).
Základný princíp
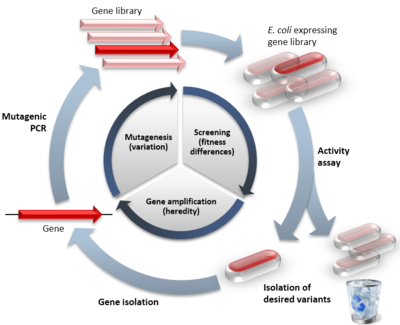
Základná myšlienka spočíva v opakovaných kolách generovania variability a následnej selekcie. Najprv sa vytvorí rozsiahla knižnica genetických variantov cieľového génu (napr. mutáciami), potom sa jednotlivé varianty exprimujú a testujú. Selekciou alebo skríningom sa izolujú gény s požadovanou funkciou; tie sa následne používajú ako vzorom pre ďalšie kolo, čím sa postupne zlepšujú vlastnosti proteínu.
Metódy vytvárania variability
Do knižnice variantov sa zvyčajne zavádzajú mutácie rôznymi prístupmi:
- Náhodná mutagenéza (napr. error-prone PCR) — spôsobí náhodné zmeny v sekvencii a je jednoduchý na implementáciu.
- Rekombinácia (DNA shuffling) — mieša časti viacerých príbuzných génov, čím kombinuje užitočné mutácie.
- Cielené zmeny (site-directed mutagenesis) — menia sa konkrétne aminokyseliny na základe štruktúrnych alebo funkčných predpokladov.
- Mutagenéza založená na údajoch — využíva sa bioinformatika alebo deep mutational scanning na riadenie, kde a aké zmeny zaviesť.
Výber a skríning
Po vytvorení knižnice je potrebné rozlíšiť zriedkavé užitočné varianty od nespočetných nefunkčných. Rozlišujeme dve hlavné stratégie:
- Selekcia — podmienka prežitia alebo rast buniek závisí od aktivity vyvíjaného proteínu (vysoko efektívna pre veľmi veľké knižnice).
- Skríning — jednotlivé klony sa testujú pomocou assay (aktivita, stabilita, väzba), často pomocou high‑throughput techník alebo automatizovaných platforiem.
Čím väčší počet mutantov sa dá otestovať, tým vyššia je pravdepodobnosť nájsť zlepšenú verziu. Moderné prístupy používajú mikrokvapôčky, mikrofluidiku a automatizované sérovacie systémy na rýchle vyhodnotenie miliónov až miliárd variantov.
In vivo vs in vitro prístupy
Môže sa to robiť in vivo (v živých bunkách baktérií alebo kvasiniek) alebo in vitro (voľne v roztoku alebo v mikrokvapkách).
Počas evolúcie in vivo sa každá bunka (zvyčajne baktéria alebo kvasinka) transformuje plazmidom obsahujúcim iný člen knižnice variantov. V jednotlivých bunkách sa líši len gén, ktorý je predmetom záujmu, pričom všetky ostatné gény zostávajú rovnaké. Bunky exprimujú proteín buď vo svojej cytoplazme, alebo na povrchu, kde sa môže testovať jeho funkcia. Tento formát má výhodu výberu vlastností v bunkovom prostredí, čo je užitočné, keď sa má vyvinutý proteín alebo RNA použiť v živých organizmoch.
Ak sa DE vykonáva bez buniek, využíva sa in vitro transkripčný a preklad na výrobu proteínov alebo RNA voľne v roztoku alebo v umelých mikrokvapôčkach. Výhodou je, že to umožňuje viac kontrolovaných podmienok (napr. vyššia alebo nižšia teplota, prítomnosť organických rozpúšťadiel), a tiež možnosť exprimovať proteíny, ktoré by boli pre bunky toxické. Okrem toho sa pri evolučných experimentoch in vitro dajú vytvoriť oveľa väčšie knižnice — často až do rádov 1015 variantov — pretože DNA knižnica sa nemusí vkladať do buniek, čo zvyčajne obmedzuje veľkosť knižnice pri in vivo metódach.
Technológie displeja a kompartimentalizácie
Pre efektívne spojenie génu s fenotypom (funkciou proteínu) existuje niekoľko etablovaných prístupov:
- Fágový displej — gén je fúzovaný s povrchovým proteínom fágov a vybraní sú fágové častice viažuce cieľ (užitočné pri vývoji väzobových proteínov a protilátok).
- Povrchový displej v kvasinkách alebo baktériách — umožňuje testovanie väzby a stability v bunkovom prostredí.
- Mikrokvapôčkové (droplet) systémy — každá kvapôčka predstavuje izolovanú reakčnú komoru, čo umožňuje vysoko paralelný skríning enzymatických aktivít; často sa využíva mikrofluidika pre rýchlu separáciu kvapôčok podľa signálu.
- Kompartimentalizovaná seba-replikácia — napr. Compartmentalized Self‑Replication (CSR), kde úspešné enzýmy katalyzujú replikáciu vlastného génu a tým sa amplifikujú.
Aplikácie a obmedzenia
Riadená evolúcia sa široko používa v:
- Priemyselnej biokatalýze (enzýmy pre potravinársky priemysel, biopalivá, čistiarne odpadových vôd).
- Vývoji terapeutických proteínov a protilátok.
- Biotechnologickom inžinierstve metabolických ciest a syntetickej biológii.
- Výskume základných mechanizmov proteínovej stability a štruktúry (mapovanie fitness krajiny).
Medzi hlavné výzvy patria:
- Potreba efektívnych, rýchlych assay na rozlíšenie malého počtu zlepšených variant z veľkých knižníc.
- Limitácie knižníc pri in vivo prístupoch (transformačná účinnosť).
- Riziko selekcie nežiaducich vedľajších vlastností (trade‑offs), napr. vyššia aktivita za cenu zníženej stability.
Postup a stratégie zlepšenia
Úspešný projekt riadenej evolúcie zvyčajne kombinuje niekoľko stratégií: začína sa širokou náhodnou knižnicou, prebieha rýchly selekčný skríning, potom nasledujú cielené mutácie alebo rekombinácia a opakované cykly. Integrácia experimentálnych dát s bioinformatikou a štrukturálnou biológiou urýchľuje identifikáciu sľubných mutácií a znižuje počet potrebných kôl.
Celkovo je riadená evolúcia silný prístup na adaptáciu a optimalizáciu proteínov v prípadoch, keď racionálny návrh sám o sebe nestačí. Kombinácia moderných vysokoparalelných techník a inteligentného návrhu experimentu umožňuje riešiť otázky, ktoré boli predtým mimo dosahu klasických metód proteínového inžinierstva.