Kovová väzba: definícia, vlastnosti, vodivosť a príklady
Kovová väzba: zrozumiteľné vysvetlenie, vlastnosti, vodivosť a príklady. Objavte, prečo kovy vedú elektrinu, majú lesk, kujnosť a vysoké teploty topenia.
Kovová väzba je typ chemického spojenia, pri ktorom sa veľké množstvo valenčných elektrónov delokalizuje a spoločné „more“ elektrónov obklopuje kladné atómové ióny. Tieto delokalizované elektróny nie sú viazané na konkrétne jadro, ale môžu sa voľne pohybovať v celej kryštalickej mriežke, čím pôsobia ako „lepidlo“, ktoré drží atómy pokope. Na rozdiel od prípadov s čistou kovalentnou alebo iónovou väzbou majú kovy zvyčajne pomerne nízku ionizačnú energiu, čo uľahčuje uvoľnenie alebo delokalizáciu valenčných elektrónov.
Elektrónové „more“ a teória pásov
Model elektrónového mora veľmi dobre vysvetľuje vlastnosti kovov: valenčné elektróny vytvárajú súvislý elektronový oblak okolo kladných iónov. Z hľadiska modernej teórie pásov sa tieto delokalizované stavy tvoria do energetických pásov (vodivostný pás a valenčný pás), pričom v kovoch sú pásy čiastočne zaplnené alebo sa prekrývajú, čo umožňuje pohyb elektrónov pri nízkych energiách.
Pevnosť, teploty topenia a mechanické vlastnosti
Intenzívna elektrostatická príťažlivosť medzi delokalizovanými elektrónmi a kladnými iónmi spôsobuje, že mnohé kovy majú vysoké teploty topenia a varu – princíp je podobný tomu pri iónových väzbách, hoci povaha väzby je odlišná. Kovová väzba je väčšinou neorientovaná (není smerovo závislá), čo umožňuje atómovým vrstvám kĺzať jednu voči druhej bez prerušenia väzieb. To vysvetľuje bežné mechanické vlastnosti kovov:
- Kujnosť (možnosť tvarovať kov tlakom bez praskania) — vďaka neorientovanej väzbe sa atómy môžu posúvať bez rozbitia štruktúry.
- Ťažnosť alebo ťažnosť (ductilita) — schopnosť byť rozťahovaný na drôt.
- Pevnosť a tvrdosť — závisia od typu kryštálovej mriežky, počtu valenčných elektrónov a prítomnosti nečistôt či zliatin.
Lesk, elektrická a tepelná vodivosť
Kovy majú charakteristický kovový lesk (lesk) preto, že delokalizované elektróny silne absorbujú a opäť vyžiaria elektromagnetické žiarenie. Voľne pohyblivé elektróny zabezpečujú aj vysokú elektrickú (elektriny) a tepelnú (vedenie tepla) vodivosť. Keď sa v kovoch pôsobí elektrické pole, elektróny sa ľahko presúvajú a vytvárajú elektrický prúd. Tepelná vodivosť je vysoká, lebo elektronický prenos energie je rýchlejší než prenos prostredníctvom vibrácií atómov (fónonov).
Väčšina kovov vykazuje nárast elektrického odporu s rastúcou teplotou (klasické správanie); niektoré kovy však pri veľmi nízkych teplotách prechádzajú do supravodivého stavu, keď odpor klesne na nulovú hodnotu.
Porovnanie s iónovými a kovalentnými väzbami
Kovové väzby sú iné než iónové (kde atómy úplne odovzdávajú elektróny a vznikajú stabilné ióny) alebo kovalentné (kde elektróny sú zdieľané medzi dvoma atómami v smerovo závislých väzbách). V kovoch sa vonkajšie energetické hladiny (atómové orbitály) prekrývajú a tvoria rozsiahle spoločné väzby. Sú tu však i podobnosti so kovalentnými väzbami, najmä keď ide o tvorbu pevných väzieb medzi atómami pri menšom počte delokalizovaných elektrónov.
Výnimky a špeciálne prípady
Neraz sa stáva, že nie všetky kovy vykazujú typickú kovovú väzbu v každom stave alebo zlúčenine. Napríklad ióny ortuti (Hg2+
2) môžu tvoriť kovalentnejšie kovovo‑kovové väzby v určitých zlúčeninách. Ďalším zaujímavým príkladom sú neokovové látky, ktoré vedú elektrický prúd: grafit vedie prúd, pretože obsahuje delokalizované π-elektróny, a iónové zlúčeniny vedú prúd, keď sú roztavené alebo rozpustené vo vode (voľné ióny).
Štruktúra a príklady
Kovy sa zvyčajne kryštalizujú v niekoľkých bežných mriežkových usporiadaniach, napríklad:
- FCC (cubická plošne centrovaná) – napr. meď, hliník, zlato
- BCC (kubická priestorovo centrovaná) – napr. železo pri izbovej teplote (alfa‑Fe)
- HCP (hexagonálna plošne centrovaná) – napr. horčík, titán
Konkrétne príklady kovov a ich využitie: meď (výborný vodič elektriny), hliník (ľahký konštrukčný kov), železo/ocel (stavebné konštrukcie), zlato a striebro (elektrická vodivosť a odolnosť voči korózii, šperkárstvo).
Zliatiny
Zliatina je homogénny roztok dvoch alebo viacerých prvkov, z ktorých aspoň jeden je kov. Zliatiny majú často lepšie mechanické vlastnosti než čisté kovy – sú tvrdšie, odolnejšie proti korózii alebo majú upravené elektrické vlastnosti. Bežné príklady:
- Brass (mosadz) – zliatina medi a zinku
- Bronz – zliatina medi a cínu
- Ocel – zliatina železa s uhlíkom a ďalšími prísadami
- Amalgámy – obsahujú ortuť a iné kovy (pozor na toxickosť ortuti)
Použitie vyplývajúce z kovových väzieb
Vlastnosti spôsobené kovovými väzbami sa využívajú v mnohých aplikáciách: elektrické vodiče, motory, tepelné výmenníky, konštrukčné materiály, elektronické komponenty, mince či šperky. Úprava zliatin a tepelných spracovaní umožňuje viesť vlastnosti presne podľa požiadaviek.
Zhrnutie: Kovová väzba vzniká delokalizáciou valenčných elektrónov a vytvorením elektronového „mora“, čo dáva kovom ich charakteristické vlastnosti — vysokú elektrickú a tepelnú vodivosť, kovový lesk, kujnosť a často vysokú pevnosť a vysoké teploty topenia. Napriek všeobecným pravidlám existujú výnimky a jemné rozdiely vysvetlené detailnejšími modelmi (pásová teória, kryštalická štruktúra, prítomnosť nečistôt a zliatin).
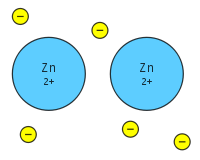
Kovové väzby sa nachádzajú v kovoch, ako je zinok.
Súvisiace stránky
- Chemická väzba
- Kovalentná väzba
- Iónová väzba
- Koordinačný komplex
- Zliatina
Otázky a odpovede
Otázka: Čo je to kovová väzba?
Odpoveď: Kovová väzba je zdieľanie mnohých oddelených elektrónov medzi mnohými kladnými iónmi, pričom elektróny pôsobia ako "lepidlo", ktoré dáva látke určitú štruktúru. Na rozdiel od kovalentnej alebo iónovej väzby.
Otázka: Prečo majú kovy nízku ionizačnú energiu?
Odpoveď: Kovy majú nízku ionizačnú energiu, pretože ich valenčné elektróny môžu byť delokalizované v rámci celého kovu, čo znamená, že nie sú spojené s konkrétnym jadrom kovu a môžu sa voľne pohybovať v celej kryštalickej štruktúre a vytvárať "more" elektrónov.
Otázka: Ako kovová väzba spôsobuje určité vlastnosti kovov?
Odpoveď: Kovové väzby spôsobujú mnohé vlastnosti kovov, ako sú pevnosť, kujnosť, ťažnosť, lesk, vedenie tepla a elektriny. Dôvodom je voľný pohyb elektrónov, ktorý umožňuje elektrickú vodivosť a rýchly prenos energie cez ne, čím vzniká elektrický prúd.
Otázka: Aký typ väzby nevykazujú všetky kovy?
Odpoveď: Nie všetky kovy vykazujú kovovú väzbu; napríklad ióny ortuti (Hg2+2) vytvárajú kovalentné väzby kov - kov.
Otázka: Čo je to zliatina?
Odpoveď: Zliatina je roztok kovov, ktorý má často podobné vlastnosti ako čisté kovy, napríklad je lesklý.
Otázka: Ako grafit vedie elektrický prúd, hoci nie je kov?
Odpoveď: Grafit vedie elektrinu, aj keď nie je kov, pretože podobne ako niektoré iné nekovy má aj on voľné elektróny, ktoré umožňujú elektrickú vodivosť.
Otázka: Existujú okrem grafitu aj iné nekovy, ktoré môžu viesť elektrický prúd?
Odpoveď: Áno, niektoré iónové zlúčeniny, ktoré sú roztavené alebo rozpustené vo vode, majú tiež voľne sa pohybujúce ióny, ktoré im tiež umožňujú viesť elektrický prúd.
Prehľadať