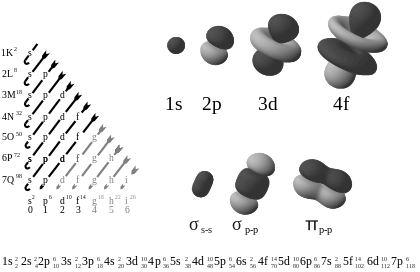
Atómové orbitaly sú miesta okolo jadra atómu, kde sa v danom okamihu s najväčšou pravdepodobnosťou nachádzajú elektróny. Je to matematická funkcia, ktorá opisuje vlnové správanie jedného elektrónu alebo dvojice elektrónov v atóme.
Slovo "orbitálny" sa používa preto, lebo sa predpokladalo, že elektróny sa správajú podobne ako slnečná sústava, kde jadro je ako Slnko a elektróny obiehajú ako planéty.
Počet atómových orbitálov v prvku je definovaný periódou, v ktorej sa prvok nachádza. Elektróny sa pohybujú medzi orbitálmi v závislosti od toho, ako rýchlo sa pohybujú a koľko je tam ďalších elektrónov.
V atómovej teórii a kvantovej mechanike je atómový orbitál kvantové číslo. Každý takýto orbitál môže byť obsadený jedným alebo dvoma elektrónmi. Spôsob usporiadania orbitálov súvisí s elektrónovými konfiguráciami atómov. Boli odvodené z opisov, ktoré poskytli prví spektroskopisti určitých spektroskopických čiar alkalických kovov ako ostré, hlavné, rozptýlené a základné.