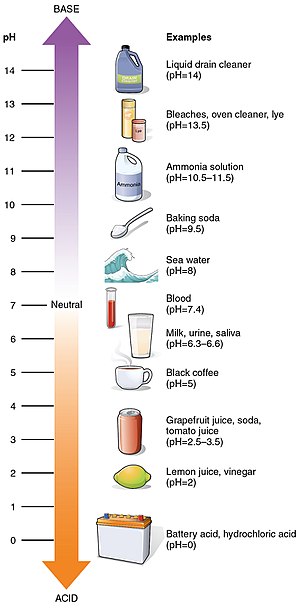
pH je stupnica kyslosti od 0 do 14. Udáva, aká je látka kyslá alebo zásaditá. Kyslejšie roztoky majú nižšie pH, zásaditejšie roztoky majú vyššie pH. Látky, ktoré nie sú kyslé ani zásadité (teda neutrálne roztoky), majú zvyčajne pH 7 pri 25 °C. Kyseliny majú pH nižšie ako 7 a zásady majú pH väčšie ako 7. pH je rýchly spôsob, ako vyjadriť koncentráciu voľných vodíkových iónov v roztoku a často sa používa v chémii, biológii, poľnohospodárstve, vodnom hospodárstve a priemysle.
pH je miera koncentrácie protónov (H+) v roztoku. S.P.L. Sørensen zaviedol tento pojem v roku 1909. Písmeno p znamená nemecký potenz, čo znamená mocnina alebo koncentrácia, a H znamená vodíkový ión (H+).
Najbežnejší vzorec na výpočet pH je:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}
[H+] označuje koncentráciu iónov H+ (často sa zapisuje aj ako [H3O+], pretože vo vode sú voľné protóny viazané ako ióny hydrónia), meria sa v móloch na liter (známe aj ako molarita). Pre praktické účely sa často uvažuje, že pH = 7 znamená neutrálny roztok pri 25 °C, pretože pri tejto teplote je autoprotolýza vody taká, že [H+] = 1×10−7 M.
Správna rovnica však v skutočnosti znie:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}
kde a H + {\displaystyle a_{\mathrm {H^{+}} }} 
Rozsah pH a extrémy
Väčšina látok má pH v rozmedzí od 0 do 14 pri bežných podmienkach (25 °C), hoci extrémne kyslé alebo zásadité roztoky môžu mať pH < 0 alebo pH > 14. Hodnota pH závisí od teploty – neutrálna voda má pH 7 iba pri približne 25 °C; pri vyššej teplote je autoprotolýza vody intenzívnejšia a hodnoty neutrálneho pH sa mierne menia.
Vzťah medzi pH a [H+] – príklady
Pre jednoduché prevody platí:
- Ak pH = 3, potom [H+] = 10−3 M = 0,001 mol·L−1.
- Ak pH = 7, potom [H+] = 10−7 M = 0,0000001 mol·L−1.
- Ak [H+] = 1×10−9 M, potom pH = 9.
Teda zmena pH o 1 jednotku znamená desaťnásobnú zmenu koncentrácie H+.
pOH, Kw a súvislosti s hydroxidmi
pH a pOH sú navzájom previazané vzťahom pH + pOH = pKw, kde Kw je ionizačná konštanta vody (pri 25 °C Kw ≈ 1,0×10−14, teda pKw = 14). Preto ak poznáte [OH−], môžete vypočítať pOH = −log10[OH−] a následne pH = 14 − pOH (pri 25 °C). Alkalické látky majú namiesto vysokých koncentrácií H+ vyššiu koncentráciu hydroxidových iónov (OH−), a ich pH je > 7.
Meranie pH
Existujú dva bežné spôsoby merania pH:
- Elektronické pH metre s sklenenou elektrodom — poskytujú presné a kvantitatívne merania; vyžadujú pravidelnú kalibráciu (minimálne v dvoch pufroch, napr. pH 4 a pH 7 alebo pH 7 a pH 10), údržbu a čistotu elektrody.
- Indikátory a indikátorové papiere (lakmus, univerzálny indikátor, fenolftaleín) — jednoduché a rýchle, vhodné pre orientačné merania. Niektoré indikátory menia farbu len v určitom rozsahu pH, preto sú menej presné než pH metre.
Pufre a Henderson–Hasselbalchova rovnica
V mnohých systémoch je dôležitá schopnosť udržať pH pri pridaní kyseliny alebo zásady — to zabezpečujú pufrové roztoky. Pre slabú kyselinu HA a jej konjugovanú zásadu A− platí Henderson–Hasselbalchova rovnica:
pH = pKa + log10([A−]/[HA])
Táto rovnica pomáha pri návrhu pufrového roztoku s požadovaným pH a vysvetľuje, prečo roztoky so správnym pomerom zásadnej a kyslej formy stabilizujú pH.
Význam pH v praxi
- Biológia a medicína: Enzymatické reakcie sú citlivé na pH; krv má úzke pH 7,35–7,45, odchýlky sú klinicky významné.
- Poľnohospodárstvo: pH pôdy ovplyvňuje dostupnosť živín pre rastliny.
- Priemysel a vodné hospodárstvo: Kontrola pH pri spracovaní vody, v chemických výrobách, pri galvanizácii a ďalších procesoch.
- Domáce využitie: pH bazénov, akvárií, čistiacich roztokov a kozmetiky.
Bezpečnosť
Silné kyseliny a zásady (veľmi nízke alebo veľmi vysoké pH) môžu byť žieravé a nebezpečné pri kontakte s pokožkou alebo očami. Pri práci s nimi používajte vhodné ochranné prostriedky (rukavice, okuliare) a dodržujte bezpečnostné postupy.
Zhrnutie
pH poskytuje jednoduchý a praktický spôsob, ako kvantifikovať kyslosť alebo zásaditosť roztoku pomocou logaritmickej stupnice založenej na koncentrácii alebo aktivite vodíkových iónov. Pri bežných riedkych roztokoch sa pH vypočítava ako pH = −log10[H+], zatiaľ čo v presnejších meraniach sa používa aktivita aH+. Meranie a kontrola pH sú kľúčové v laboratóriách, priemysle, zdravotníctve aj v každodennom živote.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)