Existuje niekoľko alotropov uhlíka. Najznámejšie sú diamant a grafit. Grafit je vodič, polokov (prvok, ktorý je čiastočne kovom a nekovom, napríklad čierny fosfor a sivý selén). Môže sa používať napríklad ako materiál v elektródach elektrických oblúkových lámp. Grafit je najstabilnejšia forma pevného uhlíka, aká bola kedy objavená.
Čo je alotropia
Alotropy sú rôzne formy toho istého chemického prvku. Všetky prvky sa skladajú jedinečne zo svojich vlastných atómov. Akékoľvek fyzikálne rozdiely sú spôsobené tým, ako sú atómy spojené. Mnohé prvky vykazujú alotropiu, pretože existuje množstvo spôsobov, ako môžu byť atómy navzájom spojené. Takisto existujú rôzne spôsoby, ako môžu byť molekuly usporiadané do väčších štruktúr.
Diamant — štruktúra, vlastnosti a použitie
Diamant je jedným z najznámejších alotropov uhlíka. Jeho atómy sú viazané v trojrozmernej sieti pomocou silných kovalentných väzieb, pričom každý uhlíkový atóm má štyri väzby v konfigurácii sp3. Táto hustá tetraedrická sieť dáva diamantu výnimočnú tvrdosť.
- Tvrdosť: diamant je najtvrdší známy prírodný minerál, čo ho robí vynikajúcim brúsivom a rezacím nástrojom pri spracovaní kovov, kameňa a keramiky.
- Optické vlastnosti: vysoký index lomu a disperzia svetla spôsobujú charakteristický lesk a „ohnivé“ záblesky, preto sa diamant široko používa v šperkoch.
- Tepelná vodivosť: diamant má veľmi vysokú tepelnú vodivosť (jedna z najvyšších u bežných materiálov), čo je užitočné pri odvode tepla v špeciálnych priemyselných aplikáciách.
- Stabilita: diamant je pri bežných podmienkach metastabilný — pri štandardných teplotách a tlakoch postupne premeniteľný na grafit, ale táto premena je extrémne pomalá.
Diamant si tiež dobre udržiava svoj lesk. Má okrem šperkárskeho aj široké priemyselné využitie — od rezacích a brúsnych nástrojov cez vŕtacie hlavy až po špecializované optické a elektronické aplikácie (napr. syntetické diamanty v elektronike, využitie NV centra v kvantových technológiách). Moderné techniky výroby syntetických diamantov zahŕňajú HPHT (vysoký tlak, vysoká teplota) a CVD (chemické napaľovanie z pár), čím sa rozširujú možnosti priemyselného použitia.
Grafit — štruktúra, vlastnosti a použitie
Grafit má úplne odlišnú štruktúru než diamant: atómy uhlíka sú tu viazané v rovinách šesťčlenných kruhov (uhlíkových šesťuholníkoch) s väzbami typu sp2. Riadky týchto vrstiev (grafénových listov) sú medzi sebou spojené len slabými van der Waalsovými silami, takže vrstvy sa ľahko od seba delia.
- Elektrická vodivosť: v dôsledku delokalizovaných π-elektrónov v rovinách je grafit dobrým vodičom elektrického prúdu v rovine vrstiev — preto je vodič, a používa sa napríklad ako materiál v elektródach elektrických oblúkových lámp alebo v batériách a elektrochemických článkoch.
- Lubrikant a tuha: ľahké oddeľovanie vrstiev robí grafit dobrým suchým mazivom a základom tuhy v ceruzkách (tzv. „grafitová tuha“).
- Tepelná stabilita a použitie v jadrovej technike: grafit odoláva vysokým teplotám a používa sa v žiaruvzdorných materiáloch aj ako moderátor v niektorých typoch jadrových reaktorov.
- Stabilita pri normálnych podmienkach: grafit je za bežných podmienok termodynamicky najstabilnejšou formou pevného uhlíka.
Ďalšie alotropy uhlíka
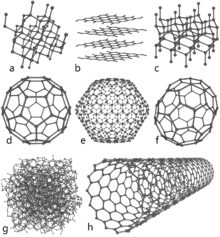
Okrem diamantu a grafitu existujú aj ďalšie významné formy uhlíka:
- Grafén: jednovrstvový, jednojadrový list uhlíkovej siete (jedna vrstva grafitu). Má výnimočnú pevnosť, vysokú elektrickú a tepelnú vodivosť a je predmetom intenzívneho výskumu.
- Fullerény: molekuly tvorená uzavretými guľovými alebo elipsoidnými reťazcami uhlíkových atómov (napr. C60 „buckyball“). Majú zaujímavé chemické a fyzikálne vlastnosti a aplikácie v materiáloch a medicíne.
- Uhlíkové nanotrubice: valcovité štruktúry odvodené od grafénu, s extrémnou pevnosťou a jedinečnými elektrickými vlastnosťami — využiteľné v elektronike, kompozitoch a senzoroch.
- Amorfický uhlík: kovy, sadze, uhlie — nekrystalické formy uhlíka bez pravidelnej dlhodochý štruktúry.
Prečo majú rôzne vlastnosti?
Rôzne vlastnosti allotropov uhlíka sú dôsledkom rozdielnej väzbovej geometrie atómov uhlíka (sp3 vs. sp2 a ďalšie) a usporiadania týchto väzieb do rôznych trojrozmerných alebo plošných štruktúr. Aj keď ide o ten istý prvok, výsledné fyzikálne a chemické vlastnosti môžu byť extrémne rozdielne — od najtvrdšieho prírodného materiálu (diamant) po dobrý elektrický vodič a mäkký lubrikant (grafit).
Zhrnutie využitia
- Diamant: šperky, brúsne a rezné nástroje, optické prvky, špecializovaná elektronika, kvantové senzory.
- Grafit: elektródy, mazivá, tuhy do ceruziek, žiaruvzdorné materiály, moderátory v reaktoroch, surovina pre výrobu grafénu a nanotubíc.
- Grafén, nanotubice, fullerény: pokročilé materiály pre elektronikou, nanotechnológie, kompozity a medicínske aplikácie.
Obe hlavné formy — diamant i grafit — majú extrémne vysoký bod topenia (v praxi uhlík sublimuje pri veľmi vysokých teplotách), čo je u nekovového prvku neobvyklé a odráža silu uhlíkových kovalentných väzieb vo vnútri ich štruktúr.