Aminokyseliny sú stavebnými prvkami bielkovín. V eukaryotoch existuje 20 štandardných aminokyselín, z ktorých sa tvoria takmer všetky bielkoviny.
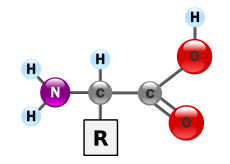
V biochémii je aminokyselina akákoľvek molekula, ktorá má aminové (NH2+R) aj karboxylové (C=O) funkčné skupiny. V biochémii sa tento termín vzťahuje na alfa-aminokyseliny so všeobecným vzorcom H2NCHRCOOH, kde R je jedna z mnohých bočných skupín (pozri schému).
Je známych približne 500 aminokyselín. Pre živočíchy sú najdôležitejšie aminokyseliny, z ktorých sa vytvárajú bielkoviny, čo sú veľmi dlhé reťazce aminokyselín. Každý proteín má svoju vlastnú sekvenciu aminokyselín a táto sekvencia spôsobuje, že proteín má rôzne tvary a rôzne funkcie. Aminokyseliny sú ako abeceda pre bielkoviny; hoci máte len niekoľko písmen, ak ich spojíte, môžete vytvoriť mnoho rôznych viet.
Deväť z 20 štandardných aminokyselín sú pre človeka "esenciálne" aminokyseliny. Ľudské telo si ich nedokáže vytvoriť (syntetizovať) z iných zlúčenín, a preto ich musí prijímať potravou. Ostatné môžu byť nevyhnutné pre niektoré vekové kategórie alebo zdravotné stavy. Esenciálne aminokyseliny sa môžu líšiť aj medzi jednotlivými druhmi. Bylinožravce musia získavať esenciálne aminokyseliny zo svojej stravy, ktorú u niektorých druhov tvorí takmer výlučne tráva. Prežúvavce, ako napríklad kravy, získavajú niektoré aminokyseliny prostredníctvom mikróbov v prvých dvoch komorách žalúdka.
Štruktúra aminokyselín
Aminokyselina alfa-typu má centrálny alfa-uhlík viazaný na štyri skupiny: aminovú (-NH2), karboxylovú (-COOH), vodík (H) a bočnú skupinu (R). Bočná skupina R určuje chemické vlastnosti každej aminokyseliny — napríklad či je hydrofóbna, hydrofilná, kyslá alebo zásaditá. Väčšina biologických aminokyselín je chirálna (má enantioméry L a D); bielkoviny v organizmoch sú zložené takmer výlučne z L-aminoacids (okrem glycínu, ktorý je achirálny).
Pri fyziologickom pH (cca 7,4) existujú aminokyseliny väčšinou ako zwitterióny — karboxylová skupina je deprotonovaná (COO-) a aminová skupina je protonovaná (NH3+). Hodnoty pKa pre karboxylové a aminové skupiny určiujú izoelektrický bod (pI) každej aminokyseliny a ovplyvňujú jej rozpustnosť a nabitie v rôznych prostrediach.
Druhy postranných skupín (R) — prehľad
- Nepolarne (hydrofóbne): glycín (glycín), alanín, valín, leucín, izoleucín, metionín, fenylalanín, tryptofán, prolín.
- Polárne, nenasýtené (neiónové): sérín, treonín, cysteín, tyrozín, asparagín, glutamín — majú schopnosť tvoriť vodíkové väzby.
- Kyslé (negatívne nabité): kyselina asparágová (aspartát), kyselina glutámová (glutamát).
- Zásadité (pozitívne nabité): lyzín, arginín, histidín (histidín môže byť čiastočne nabitý pri fyziologickom pH a často hrá dôležitú úlohu v aktívnych miestach enzýmov).
Okrem 20 štandardných proteínotvorných aminokyselín existujú aj tzv. neproteínogénne aminokyseliny (okolo 500 popísaných), medzi nimi napr. selenocysteín a pyrrolysín, ktoré sa v niektorých organizmoch vkladajú do bielkovín ako „21. a 22. aminokyselina“ za špeciálnych podmienok.
Vznik peptidovej väzby a úrovne štruktúry bielkovín
Aminokyseliny sa spájajú peptidovými väzbami — kondenzáciou karboxylovej skupiny jednej aminokyseliny s aminovou skupinou druhej (uvolní sa voda). Reťazec začína N-terminálnym (aminovým) koncom a končí C-terminálnym (karboxylovým) koncom.
Štruktúra bielkovín sa často rozdeľuje na:
- Primárna — poradí aminokyselín v reťazci (sekvencia).
- Sekundárna — pravidelné lokálne štruktúry ako alfa-helix a beta-skladaný list, stabilizované vodíkovými väzbami.
- Terciárna — trojrozmerné zloženie jedného polypeptidu, ovplyvnené hydrofóbnymi interakciami, disulfidovými mostíkmi, iontovými väzbami a van der Waalsovými silami.
- Kvaternárna — usporiadanie viacerých podjednotiek v komplexnom proteíne (napr. hemoglobín).
Funkcie aminokyselín a bielkovín
Bielkoviny plnia široké spektrum funkcií: enzýmy katalyzujú biochemické reakcie, štrukturálne proteíny (kolagén, keratín) dávajú tkanivám pevnosť, transportné proteíny (hemoglobín, transportéry membrán) prenášajú látky, receptory a signálne molekuly sa podieľajú na bunkovej komunikácii, imunoglobulíny zabezpečujú imunitnú odpoveď. Aminokyseliny tiež slúžia ako zdroj dusíka, predchodcovia neurotransmiterov (napr. glutamát → GABA) a metabolických medziproduktov.
Esenciálne aminokyseliny a výživa
Pre človeka sú obvykle považované za esenciálne tieto aminokyseliny: histidín, izoleucín, leucín, lyzín, metionín, fenylalanín, treonín, tryptofán a valín. Ich zoznam sa môže líšiť podľa veku, zdravotného stavu alebo medzi rôznymi druhmi. Niektoré aminokyseliny môžu byť podmienečne esenciálne (napr. arginín, ktoré je potrebné pri raste alebo pri ochoreniach).
Dobrými potravinovými zdrojmi kompletných proteínov (obsahujúcich všetky esenciálne aminokyseliny) sú mäso, ryby, vajcia, mliečne výrobky a sója. Rastlinné zdroje môžu byť neúplné, preto sa v rastlinnej strave odporúča kombinovať rôzne zdroje (napr. obilniny + strukoviny), aby sa dosiahla kompletnosť aminokyselinového profilu.
Biosyntéza, metabolizmus a špecifiká u rôznych druhov
Organizmy syntetizujú aminokyseliny rôznymi cestami; tie, ktoré si organizmus nedokáže vytvoriť, sú označované ako esenciálne. Ako už bolo spomenuté, prežúvavce, napr. kravy, získavajú niektoré aminokyseliny zo syntézy mikróbov v žalúdku (mikróbov), takže ich nutričné požiadavky sa líšia od iných bylinožravcov.
Okrem toho sú aminokyseliny často modifikované po-translačne (fosforylácia, glykozylácia, acetylácia, ubiquitinácia a pod.), čo rozširuje ich funkčnú variabilitu a reguluje aktivitu a lokalizáciu proteínov.
Analytické a praktické aspekty
Sekvenovanie proteínov a analýza aminokyselinového zloženia sa vykonávajú metódami ako hmotnostná spektrometria, chromatografia (HPLC) alebo genetická analýza (preklad genetickej informácie — kodóny — do konkrétnych aminokyselín). Poznanie sekvencie aminokyselín a ich chemických vlastností je základom pre porozumenie funkcie proteínov, dizajn liečiv a biotechnologické aplikácie (enzýmový inžiniering, syntéza rekombinantných proteínov).
Stručne povedané, aminokyseliny sú kľúčové molekuly života — tvoria proteíny, regulujú metabolizmus a umožňujú široké spektrum biologických funkcií. Ich rozmanitosť v bočných reťazcoch a chemických vlastnostiach umožňuje vytváranie veľmi špecifických a komplexných štruktúr a mechanizmov v živých organizmoch.