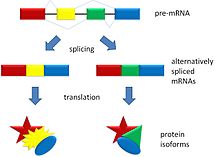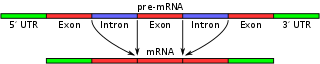
Alternatívne spájanie (splicing) umožňuje, aby z jedného génu vzniklo viacero rôznych messengerových RNA a tým aj rôznych proteínových izoforiem. Pri ňom sa zmení zloženie exónov v pre-mRNA tak, že niektoré exóny môžu byť zahrnuté alebo vynechané, alebo môžu byť použité iné miesta spájania.
Mechanizmus spájania
Spájanie prebieha v nukleáre pomocou veľkého komplexu zvaného splicozóm. Splicozóm sa skladá z malých jadrových ribonukleoproteínov (snRNP, napr. U1, U2, U4/U6·U5) a mnohých proteínových faktorov. Základné kroky sú:
- rozpoznanie 5' miesta spájania (zvyčajne začína sekvenciou GU),
- rozpoznanie vetvového bodu obsahujúceho adenín (branch point),
- viazanie 3' miesta spájania (zvyčajne končí sekvenciou AG) a polypyrimidínového traktu pred ním,
- dva transesterifikačné kroky, pri ktorých sa intrón odstráni vo forme lariatovej slučky a exóny sa spoja.
Spájanie je často ko-transkripčné — prebieha súčasne s transkripciou RNA polymerázou II. Výber miesta spájania závisí od sekvenčných signálov (konsenzusové sekvencie) a od regulačných proteínov.
Typy alternatívneho spájania
- Preskok exónu (exon skipping) – najčastejší typ, exón môže byť v niektorých transkriptoch vynechaný.
- Mutuálne exkluzívne exóny – z dvoch (alebo viacerých) exónov sa zahrnie vždy len jeden.
- Alternatívne 5' alebo 3' miesto spájania – použitie rôznych hraníc exónu, čo mení dĺžku exónu.
- Zachovanie intrónu (intron retention) – intrón zostane v zrelom mRNA a môže meniť čítací rámec alebo viesť k degradácii mRNA.
- Alternatívne začiatky transkripcie a alternatívna polyadenylácia môžu viesť k rôznym 5' alebo 3' UTR a tak nepriamo ovplyvniť alternatívne spájanie.
Regulácia spájania
Regulácia je komplexná a závisí od:
- cis-regulačných prvkov v RNA — exónové/intronové splicingové enhancery (ESE, ISE) a silencery (ESS, ISS), ktoré vplývajú na viazanie regulačných proteínov,
- trans-acting faktorov — najmä SR proteíny (serín/arginín bohaté) ako aktivátory a hnRNP proteíny ako často represory,
- rôznych bunkových stavov — vývojové štádium, typ tkaniva, signálne dráhy, rýchlosť transkripcie či posttranslačné modifikácie splicingových faktorov.
Význam a dôsledky
Alternatívne spájanie dramaticky zvyšuje proteínovú diverzitu bez potreby väčšieho počtu génov. U človeka je približne 95 % multiexónových génov alternatívne zostrihaných, čo umožňuje tkanivovo špecifické izoformy, reguláciu lokalizácie proteínov, ich funkcie a interakcií. Tiež prispieva k evolučnej flexibilite — malé zmeny v splicovacej regulácii môžu viesť k novým variáciám proteínov.
Alternatívne spájanie a choroby
Poruchy spájania často vedú k ochoreniam. Mnohé genetické poruchy sú spôsobené mutáciami, ktoré menia normálne miesta spájania alebo cis-regulačné prvky. Príklady:
- Spinálna svalová atrofia (SMA) — rozdielne spájanie génu SMN2 ovplyvňuje hladinu funkčného SMN proteínu; liek nusinersen (antisense oligonukleotid) modifikuje spájanie SMN2 a zlepšuje príznaky.
- Beta-talasémia — mnohé mutácie spôsobujú abnormálne spájanie globínových génov.
- Rôzne typy rakoviny môžu byť podporené abnormálnymi izoformami (napr. alternatívne spájanie génov regulujúcich apoptózu alebo rast), čo mení bunkové signálovanie a proliferáciu.
Kontrola kvality a osudy chybných transkriptov
Nefunkčné alebo abnormálne produkty spájania sú často rozpoznané a odstránené pomocou posttranskripčných kontrolných mechanizmov. Najdôležitejšia je nonsense-mediated decay (NMD), ktorá degraduje mRNA s predčasným stopkodónom. Okrem toho sa chybné alebo nadbytočné RNA môžu štiepiť pomocou rôznych enzýmov a exozómov.
Výskum a terapeutické prístupy
Metódy ako RNA-sekvencovanie (RNA-seq), RT-PCR a minigény umožňujú mapovať a študovať alternatívne spájanie. Terapeutické stratégie zahŕňajú:
- antisense oligonukleotidy (ASO) na presmerovanie spájania (napr. nusinersen),
- malé molekuly modulujúce splicingové faktory,
- genová terapia alebo editovanie založené na CRISPR na nápravu splicingových mutácií.
Zhrnutie
Alternatívne spájanie je kľúčový mechanizmus eukaryotov, ktorý rozširuje funkčný potenciál genómu tvoriac mesačné množstvo izoforiem z jedného génu. Regulácia je riadená kombináciou sekvenčných signálov a trans-aktívnych faktorov a jej poruchy môžu viesť k závažným chorobám. Moderná molekulárna medicína už využíva pochopenie spájania pri vývoji cielenej terapie.