Elektrónová konfigurácia je usporiadanie elektrónov v atóme. Popisuje, v ktorých orbitálov sa elektróny nachádzajú a ako sú tieto orbitály zaplnené. Štruktúra periodickej tabuľky prvkov je čiastočne založená na elektrónovej konfigurácii, pretože konfigurácia určuje chemické vlastnosti a reakčnú schopnosť prvkov.
Základné pojmy
Elektrónová konfigurácia sa riadi súborom kvantových čísel a pravidiel kvantovej mechaniky. Najdôležitejšie pojmy sú:
- Hlavné kvantové číslo (n) – určuje energetickú hladinu alebo školu (shell): n = 1, 2, 3, ...
- Vedľajšie (angl. orbitálne) kvantové číslo (l) – určuje typ podštruktúry (subshellu): l = 0 (s), 1 (p), 2 (d), 3 (f).
- Magnetické kvantové číslo (m_l) – určuje orientáciu konkrétneho orbitálu v priestore (napr. p_x, p_y, p_z).
- Spinové kvantové číslo (m_s) – určuje smer spinu elektrónu: +1/2 alebo −1/2.
Typy orbitálov a ich kapacita
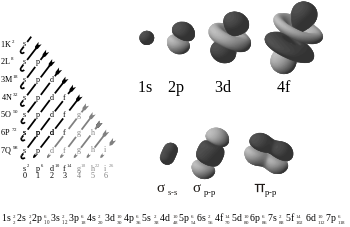
Existujú štyri najdôležitejšie typy orbitálov používané pri popise bežných prvkov:
- s – tvar približne guľový; každá s podštruktúra môže obsahovať maximálne 2 elektróny.
- p – tvar „činky“ alebo dvoch lalokov; p podštruktúra má 3 orbitály (p_x, p_y, p_z) a môže obsahovať maximálne 6 elektrónov.
- d – zvyčajne tvary pripomínajúce štvorlístok; d podštruktúra má 5 orbitálov, spolu až 10 elektrónov.
- f – komplikované tvary; f podštruktúra má 7 orbitálov, spolu až 14 elektrónov.
Pravidlá zapĺňania
Pri zostavovaní elektrónovej konfigurácie sa používajú tieto základné pravidlá:
- Pauliho vylučovací princíp – v jednom orbitáli nemôžu byť dva elektróny so všetkými rovnakými kvantovými číslami; teda každý orbitál môže obsahovať max. 2 elektróny s opačným spinom.
- Aufbau princíp (princíp zapĺňania) – orbitály sa zapĺňajú v poradí rastúcej energie; bežné poradie je: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f < 6d ... (poradie môže pri niektorých prvkoch kolísať).
- Hundovo pravidlo – pri zapĺňaní viacerých degnerovaných orbitálov (napr. tri p orbitály) sa do každého orbitálu najprv umiestni jeden elektrón s rovnakým spinom, až potom sa začínajú párovať.
Notácia elektrónovej konfigurácie
Bežná notácia uvádza hlavné kvantové číslo, typ podštruktúry a počet elektrónov v nej, napríklad:
- Vodík: 1s1
- Hélium: 1s2
- Uhlík: 1s2 2s2 2p2
- Kyslík: 1s2 2s2 2p4
Pre ťažšie prvky sa často používa skrátená (neónová alebo argónová) notácia s urovnaním vzácnych plynov v hranatých zátvorkách, napr. železo: [Ar] 4s2 3d6.
Valenčné elektróny a chemické vlastnosti
Valenčné elektróny sú elektróny v najvyššej zaplnenej energetickej hladine (n) a rozhodujú o väzbových a chemických vlastnostiach prvku. Prvky v rovnakom stĺpci periodickej tabuľky majú často rovnaký počet valenčných elektrónov a podobné chemické správanie.
Periodita a výnimky
Periodické opakovanie konfigurácií spôsobuje periodické vlastnosti prvkov (reaktivita, ionizačná energia, atómový polomer a pod.). Existujú však známe výnimky od pravidla zapĺňania, najmä medzi prechodovými prvkami, kde jemné energetické rozdiely medzi 4s a 3d (alebo 5s/4d, 6s/4f/5d) vedú k netypickým konfiguráciám. Najznámejšie príklady:
- Chrom (Cr): očakávané [Ar] 4s2 3d4, skutočné [Ar] 4s1 3d5 (poloplné d-podštruktúry sú energeticky stabilnejšie).
- Meden (Cu): očakávané [Ar] 4s2 3d9, skutočné [Ar] 4s1 3d10 (plná d-podštruktúra je stabilnejšia).
Praktické použitie
Pochopenie elektrónových konfigurácií pomáha pri predpovedaní väzieb, oxidačných stavov, magnetických vlastností a spektrálnych čiar. Konfigurácie tiež vysvetľujú, prečo majú kovy voľné elektróny vedúce k vodivosti, prečo sú vzácne plyny chemicky inertné (úplné s a p podštruktúry) a prečo majú prechodové prvky rôzne farebné zlúčeniny.
Stručné zhrnutie: elektrónová konfigurácia popisuje rozloženie elektrónov v orbitáloch (s, p, d, f), riadi sa Pauliho princípom, Aufbauovým princípom a Hundovým pravidlom, a tvorí základ pre pochopenie periodických a chemických vlastností prvkov.