V chémii a fyzike vysvetľuje atómová teória, ako sa naše chápanie atómu časom zmenilo. Kedysi sa atómy považovali za najmenšie častice hmoty. V súčasnosti je však známe, že atómy sa skladajú z protónov, neutrónov a elektrónov. Tieto subatomárne častice sa skladajú z kvarkov. Prvá myšlienka atómu pochádza od gréckeho filozofa Demokrita. Mnohé myšlienky modernej teórie pochádzajú od Johna Daltona, britského chemika a fyzika.
Teória sa vzťahuje na pevné látky, kvapaliny a plyny, ale neplatí analogicky pre plazmu alebo neutrónové hviezdy.
Definícia atómu
Atóm je základná jednotka chemického prvku, ktorá zachováva jeho chemické vlastnosti. Skladá sa z kladného jadra (nukleónov) obklopeného záporným elektrónovým obalom. Hmotnosť atómu je sústredená takmer výlučne v jadre, zatiaľ čo jeho chemické a fyzikálne vlastnosti určuje usporiadanie elektrónov v obale.
Krátka história atómovej teórie
- Antika: Demokritos (okolo 5. st. pred Kr.) navrhol myšlienku nedeliteľných častíc — „atómov“.
- Dalton (začiatok 19. st.): oživil myšlienku atómu v kontexte chemických reakcií a zákonov slučovania látok.
- Thomson (1897): objav elektrónu — „plum-pudding“ model atómu so zápornými elektrónmi v kladnom prostredí.
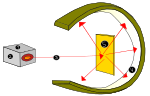
- Rutherford (1911): experiment s alfa časticami ukázal, že atóm má malé, husté, kladné jadro.
- Bohr (1913): kvantovanie energetických hladín pre elektrón v atóme vodíka — úspešný pre spektrálne čiary, ale obmedzený pre zložitejšie atómy.
- Moderná kvantová mechanika (1920–30): Schrödinger, Heisenberg a ďalší nahradili klasické dráhy pravdepodobnostnými vlnovými funkciami a orbitálmi.
- Chadwick (1932): objav neutróna, čo vysvetlilo štiepenie atómových hmotností a izotopy.
- Teória kvarkov (1960s): Gell‑Mann a Zweig opísali proklamované kvarky ako konštrukčné súčasti protónov a neutrónov.
Vnútorná stavba atómu
Atóm má dve základné časti: jadro a elektrónový obal.
Jadro
- Protóny — kladne nabité častice; ich počet určuje atómové číslo Z a identitu prvku.
- Neutróny — neutrálne častice; spolu s protónmi určujú nukleónové číslo (hmotnostné číslo A).
- Jadrové sily — protóny a neutróny v jadre drží silná jadrová sila (založená na silnej interakcii), ktorá prekonáva elektrostatické odpudzovanie medzi protónmi.
- Veľkosť a hmotnosť: typický polomer jadra je približne 10⁻¹⁵ m (femtometer), zatiaľ čo celkový atóm má rozmer rádovo 10⁻¹⁰ m. Jadro obsahuje takmer všetku hmotnosť atómu.
- Rádioaktivita a stabilita: nadbytok alebo deficit neutrónov môže viesť k rádioaktívnym premenám (alfa, beta, gama). Energetická väzba v jadre sa meria väzbovou energiou na nukleón.
Elektrónový obal
- Elektróny — záporné častice s veľmi malou hmotnosťou v porovnaní s nukleónmi; určujú chemické vlastnosti a väzby prvkov.
- Elektrónové hladiny a orbitály: elektróny obsadzujú kvantované energetické hladiny (škrupiny označované K, L, M...). V rámci hladín sú orbitály (s, p, d, f), ktoré popisuje kvantová mechanika pomocou vlnovej funkcie.
- Kvantové čísla: hlavné kvantové číslo n, vedľajšie l, magnetické m a spinové s definujú stav elektrónu v atóme. Platí Pauliho vylučovací princíp — v jednom atóme neexistujú dva elektróny so všetkými štyrmi rovnakými kvantovými číslami.
- Elektrónová konfigurácia: určuje usporiadanie elektrónov a teda reaktivitu, tvorbu väzieb a umiestnenie prvkov v periodickej tabuľke.
Subnukleárne častice a kvarky
Protóny a neutróny sú zložitejšie častice zložené z kvarkov. Každý protón pozostáva z dvoch up (u) a jedného down (d) kvarku (uud), zatiaľ čo neutron je zložený z jedného u a dvoch d kvarkov (udd). Kvarky sú viazané silnou interakciou sprostredkovanou gluónmi.
Izotopy, ióny a chemické dôsledky
- Izotopy: atómy toho istého prvku majú rovnaký počet protónov, ale rôzny počet neutrónov (napr. uhlík‑12, uhlík‑14). Izotopy sa líšia hmotnosťou a rádioaktivitou, často sa využívajú v datovaní a medicíne.
- Ióny: vznikajú stratou alebo získaním elektrónov; kationty sú kladne nabité (strata elektrónov), anióny záporne (zisk elektrónov). Ióny výrazne menia chemické vlastnosti látok.
Modely atómu — stručné porovnanie
- Daltonov model: atómy pevné guľôčky, nedeliteľné (historický význam).
- Thomsonov model: elektróny v kladnom „obláčiku“.
- Rutherfordov model: malé jadro, elektróny obiehajú okolo (planetárny obrázok jadra).
- Bohrův model: kvantované dráhy elektrónov — vysvetlil spektroskopiu vodíka.
- Kvantovo-mechanický model: moderný obraz založený na vlnových funkciách a pravdepodobnostiach, ktorý spoľahlivo opisuje väčšinu vlastností atómov.
Výnimky a špeciálne stavy
Atómová teória a modely, ktoré z nej vychádzajú, sa primárne týkajú normálnych stavov hmoty — pevné látky, kvapaliny, plyny. Existujú však stavy, kde klasický obraz atómu už neplatí alebo je výrazne pozmenený:
- Plazma: pri vysokých teplotách sú atómy čiastočne alebo úplne ionizované; elektróny a ióny sa správajú ako voľné nabité častice.
- Neutrónové hviezdy: v extrémnych hustotách môže hmota prejsť do stavu, kde dominujú neutróny alebo dokonca exotické formy hustej kvarkovej hmoty — klasický atóm tu neexistuje.
Použitie a význam
Pochopenie atómovej štruktúry umožňuje:
- vysvetliť chemické reakcie a tvorbu väzieb,
- využiť spektroskopiu pri určovaní zloženia látok,
- vyvíjať materiály, lieky a nanotechnológie,
- využiť jadrovú energiu a rádioizotopy v medicíne a priemysle.
Zhrnutie
Atómová teória sa vyvíjala od filozofických predstáv cez jednoduché modely až po sofistikovanú kvantovú mechaniku. Moderný obraz atómu rozlišuje jadro (protóny a neutróny) a elektrónový obal, pričom ďalšie úrovne štruktúry odhaľujú kvarkovú povahu nukleónov. Tento obraz platí pre bežné formy hmoty, avšak v extrémnych podmienkach (plazma, neutrónové hviezdy) je potrebné uvažovať o odlišných fyzikálnych režimoch.