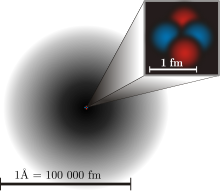
Model slivkového pudingu bol skorým (a nesprávnym) modelom atómu z 20. storočia. Navrhol ho J. J. Thomson v roku 1904, po objavení elektrónu, ale pred objavením atómového jadra. V tom čase vedci vedeli, že v atóme je kladný náboj, ktorý vyvažuje záporné náboje elektrónov, takže atóm je neutrálny, ale nevedeli, odkiaľ sa kladný náboj berie. Thomsonov model zobrazoval atóm, ktorý mal kladne nabité prostredie alebo priestor so záporne nabitými elektrónmi vo vnútri prostredia. Krátko po jeho návrhu sa tento model nazval modelom "slivkového pudingu", pretože kladné prostredie bolo ako puding s elektrónmi alebo slivkami vo vnútri.
Charakteristika modelu
Thomsonov model popisoval atóm ako súvislé kladne nabité telo (rozloženie kladného náboja približne rovnomerné) s jednotlivými elektrónmi rozmiestnenými vnútri tak, ako sú kúsky ovocia v pudingu. Elektróny mali byť v stabilnej rovnováhe v dôsledku príťažlivých síl kladného prostredia a odpudivých síl medzi sebou. Thomson sa zaoberal aj usporiadaním elektrónov (napríklad kruhové vrstvy alebo krúžky) a skúšal odhadnúť podmienky stability a prirodzené frekvencie ich kmitania.
Prečo bol model navrhnutý
- Objav elektrónu (koncom 19. storočia) ukázal, že atómy obsahujú záporné častice, ale zdroj kladného náboja bol neznámy.
- Model poskytoval jednoduché, intuitívne vysvetlenie elektrickej neutrality atómu bez potreby malého, hustého jadra.
- Bol to prvý krok k začleneniu novoodhalených častíc do koncepcie atómu a snažil sa vysvetliť aj niektoré spektrálne či dynamické vlastnosti atómov.
Limity a experimentálne vyvrátenie
Model mal viacero zásadných problémov:
- Nepresne vysvetľoval rozptýlenie vysokoenergetických častíc pri experimentoch so žiarením.
- Nevedel uspokojivo vysvetliť ostré spektrálne čiary atómov ani ich stabilitu podľa klasickej elektrodynamiky.
- Nezhodoval sa s výsledkami pozorovaní pri rozptyle alfa častíc vykonaných geigrom, marsdenom a analyzovaných Rutherfordom (slávne Geiger–Marsdenove experimenty okolo roku 1909).
Na základe týchto experimentov Ernest Rutherford v roku 1911 navrhol model, kde je kladný náboj sústredený v malom, hustom jadre, zatiaľ čo elektróny obiehajú okolo jadra — to radikálne zmenilo predstavu o vnútri atómu a nahradilo model slivkového pudingu.
Historický význam a dedičstvo
Aj keď bol Thomsonov model nesprávny, zohral dôležitú historickú úlohu:
- Bol prvým systematickým pokusom zaradiť elektrón do modelu atómu po jeho objave.
- Podnietil presné experimenty (napr. rozptyl častíc), ktoré viedli k objavu jadra a rozvoju modernej jadrovej fyziky.
- Ilustruje, ako sa vedecké teórie postupne korigujú na základe nových dôkazov — aj chybné modely majú hodnotu tým, že kladú základy ďalším objavom.
Ďalšie kroky po Thomsonovi
Po Rutherfordovom modeli nasledoval Bohr (1913), ktorý kombinoval klasické pojmy s kvantovými postulátmi a úspešne vysvetlil spektrálne čiary vodíka. Neskôr sa vyvinula kvantová mechanika, ktorá poskytla úplnejší a presnejší opis atómov a väzieb medzi časticami.
Stručne: model slivkového pudingu je významný ako historický medzník — jednoduché a intuitívne vysvetlenie, ktoré však výsledky experimentov vyvrátili a ktoré viedlo k hlbšiemu pochopeniu štruktúry atómu.