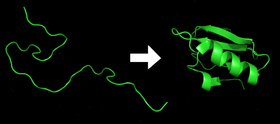
Skladanie proteínov je proces, pri ktorom proteín získava svoj funkčný tvar alebo "konformáciu". Je to hlavne samoorganizujúci sa proces: počiatočne náhodným zvitkom sa polypeptidy skladajú do svojho charakteristického funkčného tvaru, ktorý držia pohromade predovšetkým vodíkové väzby, ale aj hydrofóbne interakcie, elektrostatické väzby a disulfidické mostíky.
Základné etapy skladania
- Pri syntéze na ribozóme vzniká lineárny reťazec aminokyselín, ktorý spravidla začína v rozloženom alebo čiastočne neusporiadanom stave.
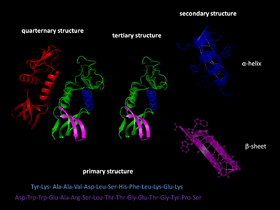
- Aminokyseliny vzájomne interagujú a postupne sa formuje presne definovaná trojrozmerná štruktúra, nazývaná natívny stav. Táto výsledná konformácia je primárne určená sekvenciou aminokyselín (Anfinsenova dogma), pričom v bunkovom prostredí môžu byť potrebné aj pomocné faktory.
Bez správnej trojrozmernej štruktúry proteín nefunguje. Niektoré regióny proteínov môžu zostať flexibilné alebo neusporiadané — to je bežné a mnohé takéto časti majú funkčnú úlohu (tzv. intrinsically disordered regions alebo proteíny).
Mechanizmy a energetická krajina skladania
Skladanie je riadené energetickou krajinou: natívny stav je obvykle termodynamicky stabilný (najnižšia voľná energia), ale cesta do tohto stavu môže prebiehať cez rýchle alebo pomalé medzistavy (molten globule, čiastočne zložené štruktúry). Problém Levinthalovho paradoxu zdôrazňuje, že proteíny neskúmajú náhodne všetky možné konfigurácie — skladanie prebieha smerovane cez kineticky a termodynamicky priaznivé dráhy (nukleácia‑kondenzácia, hierarchické zoskupovanie sekundárnych štruktúr a pod.).
Faktory ovplyvňujúce skladanie
- Primárna sekvencia: poradie a chemická povaha aminokyselín určuje možné interakcie.
- Prostredie: teplota, pH, iónová sila a prítomnosť rozpúšťadiel ovplyvňujú stabilitu štruktúr.
- Kofaktory a metalické ióny: niektoré proteíny potrebujú viazané ióny alebo malé molekuly (napr. hem, vitamíny) na správne zloženie.
- Post-translačné modifikácie: glykozylácia, fosforylácia, tvorba disulfidov a pod. môžu byť nevyhnutné pre natívny tvar.
- Bunkové stroje: chaperóny a chaperoníny pomáhajú zabrániť nežiaducemu zhlukovaniu a asistujú pri správnom sklade.
Chaperóny a udržiavanie proteínovej homeostázy
V bunke pôsobia špecializované molekuly — proteínové chaperóny (napr. Hsp70, Hsp90, Hsp60/GroEL) — ktoré zabraňujú agregácii, stabilizujú zložité medzistavy a v niektorých prípadoch poskytujú „izolačné komory“, kde sa skladanie môže bezpečne dokončiť. Ak sa proteín nevie správne zložiť, bunky ho často označia na rozklad systémom ubikvitín‑proteazóm alebo ho odstránia autophágiou — súhrnne tieto procesy nazývame proteostáza.
Keď skladanie zlyhá — dôsledky pre zdravie
Ak sa proteíny nezložia do svojho pôvodného tvaru, sú často neaktívne a môžu byť toxické. Predpokladá sa, že viaceré ochorenia sú dôsledkom nesprávne zložených proteínov. Typické príklady zahŕňajú:
- Neurodegeneratívne ochorenia: Alzheimerova choroba (amyloid‑β a tau), Parkinsonova choroba (α‑synukleín), Huntingtonova choroba (mutovaný huntingtín) — všetky spojené s tvorbou oligomérov a amyloidných fibríl.
- Prionové choroby: patologické priony konvertujú zdravú konformáciu proteínu na patogénnu formu.
- Ochorenia spôsobené chybným zložením jedného proteínu: cystická fibróza (mutovaný CFTR je nesprávne skladaný a degradovaný), nedostatok alfa‑1 antitrypsínu, transthyretínová amyloidóza.
Mnohé alergie sú tiež späté so skladaním bielkovín, pretože imunitný systém nemusí rozpoznať všetky možné konformácie a niektoré štruktúry môžu byť viac imunogénne. Okrem toho toxické intermediáty alebo agregáty môžu poškodzovať bunkové membrány, mitochondrie a spúšťať zápalové dráhy.
Štúdium skladania — metódy a prístupy
Výskumníci kombinujú množstvo experimentálnych a výpočtových metód na sledovanie skladania a chýb v skladaní:
- Štrukturálne metódy: röntgenová kryštalografia, nukleárna magnetická rezonancia (NMR), kryo‑elektrónová mikroskopia (cryo‑EM).
- Spektroskopické a kinetické metódy: kruhová dichroizmus (CD), fluorescenčné metódy vrátane FRET, stop‑flow kinetika.
- Biochemické a bunkové assay: meranie agregácie, testy stability, sledovanie degradácie proteínov v bunke.
- Výpočtové modelovanie: simulácie molekulárnej dynamiky a predikčné algoritmy pre štruktúru (napr. moderné metódy založené na strojovom učení).
Záver — prečo je skladanie dôležité
Skladanie proteínov je kľúčové pre správnu funkciu buniek a organizmu. Porozumenie mechanizmom skladania a príčinám jeho porúch umožňuje vyvíjať terapeutické prístupy: malé molekuly a farmaceutické chaperóny, zásahy podporujúce degradáciu patologických agregátov, alebo imunoterapie zamerané proti toxickým oligomérom. Preto je štúdium skladania proteínov centrálnou súčasťou molekulárnej biológie, biomedicíny a vývoja liečív.