Malá interferujúca RNA (siRNA) je trieda dvojvláknových molekúl RNA s dĺžkou 20–25 párov báz. Typické siRNA duplexy majú dve nukleotidové voľné 3' konce (2‑nt 3' presahy) a pri biologickej aktivácii sú spravidla spracované z dlhších dvojvláknových RNA molekúl enzymom Dicer.
Funkcia v RNA interferencii: siRNA zohráva kľúčovú úlohu v ceste RNA interferencie (RNAi), mechanizme, ktorým bunky znižujú expresie vybraných génov. Gény sú cielene ovplyvnené iba vtedy, ak majú nukleotidové sekvencie komplementárne k sekvencii siRNA; presnosť párovania medzi vodiacou (guide) siRNA a cieľovou mRNA určuje typ potlačenia (pri takmer dokonalom párovaní dochádza k štiepeniu mRNA, pri čiastočnom k potlačeniu translácie alebo zníženiu stability mRNA).
Mechanizmus pôsobenia
Zhruba postup pri klasickej posttranskripčnej sile RNAi:
- Vznik dlhých dvojvláknových RNA (napr. počas vírusovej replikácie alebo z vnútrobunkových prekurzorov) je spracovaný ribonukleázou Dicer na 20–25 nt siRNA duplexy.
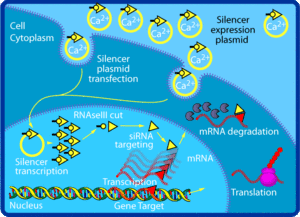
- Duplex sa načíta do proteínového komplexu RISC (RNA-induced silencing complex). Jeden z dvoch reťazcov sa vyberie ako vodiaci (guide) a druhý, tzv. passenger, sa odstráni alebo degraduje.
- Vodiaca siRNA priľne ku komplementárnej cieľovej mRNA. Proteín Argonaute (Ago2 u cicavcov) pri dokonalom alebo takmer dokonalom párovaní štiepi mRNA (typicky medzi 10. a 11. nukleotidom počítaným od 5' konca vodiaceho reťazca), čo vedie k jej degradácii a zablokovaniu transkripcii cieľového génu na funkčný produkt.
- Tým sa zabráni následnej translácii konkrétnej mRNA do proteínu, čo efektívne znižuje hladinu proteínu kódovaného dotyčným génom.
Ďalšie biologické úlohy
Okrem posttranskripčného štiepenia mRNA môže siRNA participovať v ďalších dráhach súvisiacich s RNAi: napríklad ako antivírusový mechanizmus v rastlinách a bezstavovcoch, alebo pri formovaní chromatínovej štruktúry genómu a transkripčnej inhibícii (transcriptional gene silencing) v niektorých organizmoch. Mechanizmy a regulačné väzby týchto dráh sú predmetom intenzívneho výskumu.
Rozdiel medzi siRNA a miRNA
- siRNA: často vzniká z exogénnych alebo špecifických zdrojov dvojvláknovej RNA, má vysokú komplementaritu so svojím cieľom a vedie k priamemu štiepeniu mRNA.
- miRNA: pochádza z endogénnych prekurzorov (hairpin), zväčša pôsobí pri čiastočnej komplementarite, výsledkom čoho je potlačenie translácie alebo destabilizácia mRNA bez priameho štiepenia.
Biotechnologické a terapeutické použitie
siRNA sa široko využívajú ako nástroj výskumu na selektívne „vypínanie“ génov (knockdown) a v posledných rokoch sa rozvíjajú ako terapeutické molekuly. Príklady a stratégie:
- syntetické siRNA duplexy alebo vektory exprimujúce šort‑hairpin RNA (shRNA), ktoré sa v bunke spracujú na funkčné siRNA;
- klinicky schválené terapie založené na siRNA (napr. liečby cielene zamerané na genetické ochorenia alebo poruchy metabolizmu);
- doručovacie systémy: lipidové nanočastice, chemické modifikácie nukleotidov (napr. 2'-O‑metyl, 2'-fluóro), konjugáty (napr. GalNAc pre pečeň) alebo vírusové/nezávislé transportné systémy, ktoré zlepšujú stabilitu, znížia imunitnú stimuláciu a smerujú siRNA do cieľových tkanív.
Výzvy a obmedzenia
- off‑target účinky spôsobené čiastočnou komplementaritou s inými mRNA;
- imunostimulačné odpovede na exogénnu RNA (TLR senzory, interferónová odpoveď);
- efektívne a bezpečné doručenie do konkrétnych tkanív, preklenutie biologických bariér (napr. hematoencefalická bariéra);
- dlhodobá stabilita a kontrola expresie pri génovej terapii pomocou siRNA‑podobných prístupov.
Vzhľadom na tieto výzvy sa v praxi často uplatňujú kombinované prístupy: starostlivý dizajn sekvencií, chemické modifikácie, optimalizované formulácie doručenia a rozsiahle testovanie špecifickosti. Výskum siRNA pokračuje rýchlym tempom a prináša nové poznatky o mechanizmoch RNAi, biologických úlohách siRNA a ich potenciáli v medicíne a biotechnológii.