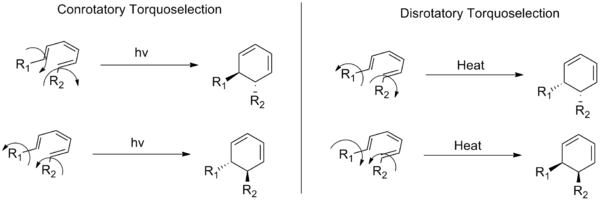
Konrotácia a disrotácia sú dva základné stereochemické priebehy elektrocyklických reakcií, teda jedného typu organických chemických reakcií). V týchto reakciách sa uzatvára alebo otvára kruh v konjugovanom systéme a smer otáčania koncov reťazca rozhoduje o tom, aký stereochemický produkt vznikne.
Čo je konrotácia
Pri konrotácii sa substituenty na koncoch konjugovaného systému dvojitých väzieb pohybujú v rovnakom smere, či už v smere alebo proti smeru hodinových ručičiek), počas otvárania alebo uzatvárania kruhu. Tento priebeh je stereospecifický, čo znamená, že zo štruktúry východiskovej látky možno pomerne presne predpovedať konfiguráciu produktu.
Čo je disrotácia
V disrotačnom režime sa koncové časti systému otáčajú v opačných smeroch. Aj tu ide o stereospecifický dej, ale výsledok je odlišný od konrotácie. Rozdiel medzi oboma režimami je dôležitý najmä pri predpovedaní, či vznikne cis alebo trans usporiadanie substituentov v konečnom cyklickom produkte.
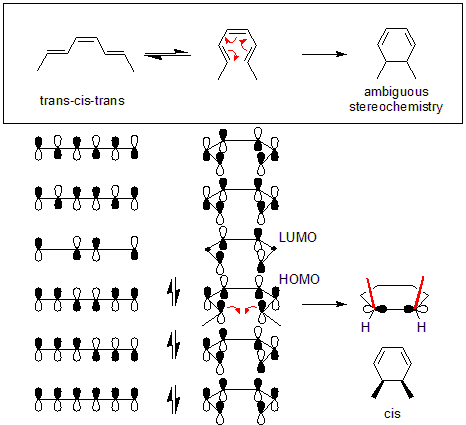
Príkladom je premena trans-cis-trans-2,4,6-oktatriénu na cis-dimetylcyklohexadién (horná časť obrázka). Orbitálna mechanika reakcie si vyžaduje disrotačný režim. Orbitálna symetria najvyššie obsadeného molekulového orbitálu oktatriénu (HOMO) vyžaduje, aby sa koncové pi orbitály pohybovali v opačných smeroch, aby sa vytvorila správna symetria, ktorá sa nachádza v sigma väzbe.
Pravidlá podľa typu elektrónového systému
Tepelné prestavby všetkých konjugovaných systémov obsahujúcich 4n + 2 π elektrónov sú stereošpecifické a zvyčajne prebiehajú disrotáciou. Naopak, systémy obsahujúce 4n π elektrónov vykazujú konrotačný režim. Platí to aj pre preskupenia 4n + 2 π (kde n je celé číslo) elektrónov riadené svetlom (fotoindukované). Fotoindukované preskupenia systémov so 4n π elektrónmi (kde je počet elektrónov deliteľný 4) sa riadia disrotáciou.
Inými slovami, pri elektrocyklických reakciách sa smer otáčania mení podľa toho, či reakcia prebieha tepelne alebo fotoindukovane. Preto nestačí poznať len počet π elektrónov; vždy treba zohľadniť aj podmienky reakcie.
Prečo je to dôležité
Konrotácia a disrotácia pomáhajú chemikom predpovedať stereochémiu produktu ešte pred experimentom. To je užitočné pri návrhu syntéz, pri analýze mechanizmov a pri vysvetľovaní toho, prečo z jednej látky vzniká len určitý izomér. Tieto pravidlá sú jedným z najlepších príkladov toho, ako orbitálna symetria ovplyvňuje priebeh organických reakcií.
Woodwardove-Hoffmannove pravidlá sumarizujú vyššie uvedené rôzne reakcie a poskytujú všeobecný rámec na určenie toho, či bude elektrocyklická reakcia prebiehať konrotáciou alebo disrotáciou.
Nasledujúci obrázok tiež ukazuje rozdiel medzi konrotatívnymi a disrotatívnymi reakciami: