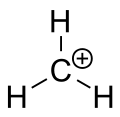
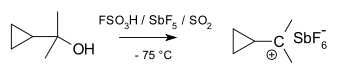
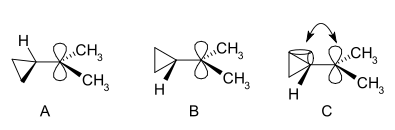
Karbocation je ión s kladne nabitým atómom uhlíka. Nabitý atóm uhlíka v karbokacióne má často len šesť elektrónov vo vonkajšej valenčnej škrupine namiesto plného oktetu; preto sa hovorí o „sextete“. Podľa pravidla oktetu sú atómy s ôsmimi valenčnými elektrónmi najstabilnejšie, a preto sa karbokátiony správajú ako veľmi reaktívne medziprodukty — snažia sa získať späť plný oktet a neutrálny náboj.
Štruktúra a hybridizácia
Aj keď by jednoduchá logika mohla naznačovať, že karbokátiony majú sp3 hybridizáciu s „prázdnym“ sp3 orbitálom, experimenty a výpočty ukazujú, že väčšina stabilných karbokátionov je sp2 hybridizovaná a planárna. To znamená, že nabitý uhlík má trigónálne planárnu geometriu a neobsadený p-orbitál kolmý na rovinu väzieb; práve tento prázdny p-orbitál prijíma elektróny pri nukleofilných útokoch.
Faktory ovplyvňujúce stabilitu
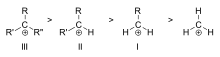
- Hyperkonjugácia: alkylové skupiny môžu delokalizovať kladný náboj cez σ–C–H väzby, čo stabilizuje kation. Preto platí poradie stability: terc. > sek. > prim. > metyl.
- Indukčný efekt: skupiny s elektron-donorovými vlastnosťami (napr. alkyly) znižujú koncentráciu kladného náboja na uhlíku.
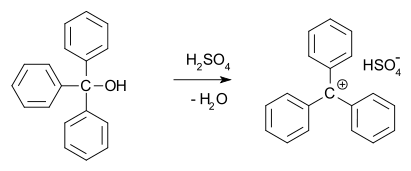
- Rezónančná delokalizácia: ak je kation susediaci s π-systémom (napr. benzylický alebo allylický karbokátion), náboj sa delokalizuje na viaceré atómy a kation je výrazne stabilizovaný.
- Elektróny darujúce substituenty: skupiny ako -OR alebo -NR2 môžu stabilizovať kation rezonančne alebo induktívne.
- Geometria a napätie: štrukturálne obmedzenia (napr. mostíkové alebo „non‑classical“ kationy) môžu viesť k neobvyklým delokalizovaným riešeniam, ktoré sú menej alebo viac stabilné podľa prípadu.
Druhy karbokátionov
- Alkylové: metylový, primárny, sekundárny, terciárny (stabilita podľa hyperkonjugácie).
- Benzylické a allylické: silne stabilizované rezonančnou delokalizáciou.
- Vinylové a arylové: vo všeobecnosti veľmi nestabilné, pretože kladný náboj nie je ľahko delokalizovateľný v rámci hybridizácie uhlíkového centra.
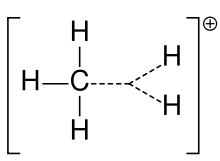
- Mostíkové alebo „non‑classical“ kationy: kedy je kladný náboj delokalizovaný cez viacero väzieb (príklad: norbornylový kation), historicky kontroverzný, dnes dobre študovaný prípad elektronickej delokalizácie.
Vznik a typické reakcie
Karbokationy sa tvoria bežne pri reakciách zahŕňajúcich heterolytické štiepenie väzby C–X (napr. odštiepenie halogenidu pri SN1), protónovaní alkenov (pri elektrofilnej adícii), pri reakciách E1 alebo pri hydride/alkylových preskokoch (rearrangements). Po svojom vzniku karbokátiony podliehajú:
- nukleofilnému útoku — vznik nových väzieb (napr. SN1),
- eliminácii (E1) — tvorba alkenov,
- rearrangements (hydridové alebo alkylové preskoky) — za účelom vytvorenia stabilnejšieho kationu,
- trappingu alebo adícii rozpúšťadla pri donorech elektrónov.
Experimentálna detekcia a životnosť
Väčšina karbokátionov sú krátkožijúce medziprodukty; ich prítomnosť sa preukazuje nepriamymi metódami (produktová analýza, stereochemické dôkazy) alebo priamymi technikami pri nízkych teplotách: nízkoteplotná NMR, kryogénne podmienky, infračervená spektroskopia a hmotnostná spektrometria. V niektorých prípadoch (silne stabilizované rezonančné kationy alebo pri dostatočnej stabilizácii rozpúšťadlom) je možné pozorovať karbokationy priamo.
Historické poznámky a moderný pohľad
Diskusia o „klasických“ vs. „neklasických“ (mostíkových) karbokátionoch bola dôležitá pre vývoj organickej chémie. Moderné experimentálne a výpočtové metódy ukázali, že mnohé prípady non‑classical charakteru sú skôr prípadmi silnej delokalizácie náboja než úplného rozdelenia väzieb — to mení naše chápanie a pomáha lepšie predpovedať reaktivity.
Reaktivita karbokationov je teda riadená ich štruktúrou a stabilitou: čím je kation stabilnejší (hyperkonjugácia, rezónancia, indukčné efekty), tým je pravdepodobnejšie, že sa bude správať ako izolovateľný alebo dlhšie trvajúci medziprodukt a tým sa mení pomer medzi možnými reakčnými cestami (nukleofilný útok vs. eliminácia vs. rearrangement).
Stručne: karbokátiony sú kľúčové a univerzálne medziprodukty v organickej chémii — ich pochopenie (štruktúra, faktory stabilizácie a reakčná schopnosť) je nevyhnutné pri predpovedaní výsledkov mnohých reakcií.