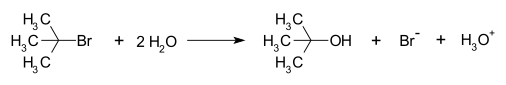
Reakcia NS1 je substitučná reakcia v organickej chémii. "SN" znamená nukleofilnú substitúciu a "1" predstavuje skutočnosť, že krok určujúci rýchlosť zahŕňa len jednu molekulu (unimolekulárna). Reakcia zahŕňa karbokačný medziprodukt. Niektoré bežnéN reakcie S1 sú reakcie sekundárnych alebo terciárnych alkylhalogenidov za silne zásaditých podmienok alebo za silne kyslých podmienok so sekundárnymi alebo terciárnymi alkoholmi. Pri primárnych alkylhalogenidoch dochádza k alternatívnej reakcii NS2. Medzi anorganickými chemikmi je reakcia NS1 často známa ako disociačný mechanizmus. Christopher Ingold a kol. prvýkrát navrhli tento reakčný mechanizmus v roku 1940.
Mechanizmus
Mechanizmus SN1 prebieha typicky dvoma základnými krokmi:
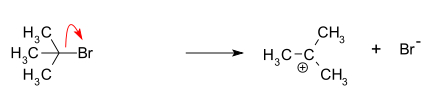
- Disociácia: Odchod odchádzajúcej skupiny (napr. halogenidu) z tvorby neutrálneho alebo nabitého produktu, ktorý vedie k vzniku karbokationtu (R–L → R+ + L−). Tento krok je pomalší a určuje rýchlosť celej reakcie.
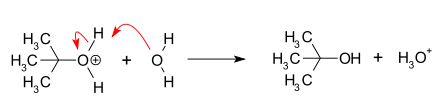
- Útok nukleofilu: Nukleofil napadá planarický karbokation a viaže sa k uhlíku, čím vzniká substitučný produkt (R+ + Nu → R–Nu). Tento krok je rýchlejší a nie je určujúci rýchlosť.
Rýchlosť reakcie SN1 zodpovedá kinetike prvého rádu, t. j. rýchlosť = k[substrát]. Narušenie tejto kinetiky (napr. v prítomnosti silných nukleofilov alebo pri špecifických substrátoch) môže viesť k zložitejšiemu správania, no štandardný model predpokladá, že nukleofil neovplyvňuje počiatočnú rýchlosť.
Stabilita karbokationtu a faktory podporujúce SN1
Karbokationty sú kľúčové pre SN1; ich stabilita rozhoduje o tom, či reakcia prebehne touto cestou. Obecné zásady:
- Terciárne karbokationty sú stabilnejšie než sekundárne, a tie sú stabilnejšie než primárne (terciárne > sekundárne > primárne).
- Resonančne stabilizované karbokationty (napr. benzylické alebo allylické) veľmi ľahko vznikajú a často podstupujú SN1.
- Solvent: polar-poltické (najmä protické) rozpúšťadlá stabilizujú vznikajúci iónový pár (R+ a L−) a teda urýchľujú disociačný krok. Preto sú polar protické rozpúšťadlá (napr. voda, alkoholy) typické pre reakcie SN1.
- Odchádzajúca skupina: lepšie odchádzajúce skupiny (napr. I−, Br−, tosylát) uľahčujú disociáciu a podporujú SN1.
Stereochemické dôsledky a preskupenia
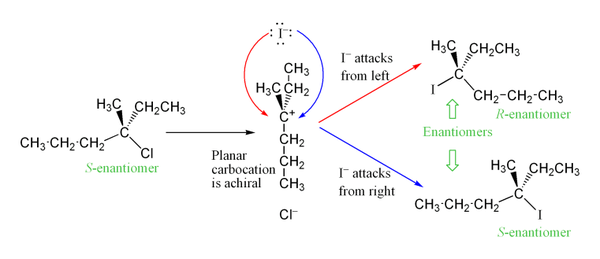
Keďže karbokation je planárny (sp2 hybridizovaný), nukleofil môže zaútočiť z oboch strán, čo často vedie k čiastočnej alebo úplnej racemizácii centra (strata striktného chirálneho usporiadania). V praxi sa však často pozoruje čiastočná retencia konfigurácie kvôli takzvanému ion-pair (solvovanému alebo nesolvovanému) – nukleofil môže zaútočiť ešte pred úplným oddelením aniónu a kationtu.
Karbokačné medzičlánky majú tendenciu podstupovať přesuny (rearrangements), napr. 1,2-hydridový alebo 1,2-alkylový presun, ak to vedie k stabilnejšiemu karbokationtu. Tieto presuny často vysvetľujú neočakávané produkty pri SN1.
Rozdiel oproti SN2 a súvisiace konkurencie
Hlavný rozdiel oproti SN2 je v mechanizme a faktoroch, ktoré reakciu riadia:
- SN1: unimolekulárny, rýchlostne nezávislý od nukleofilu, preferuje stabilné karbokationty a polar protické rozpúšťadlá.
- SN2: bimolekulárny (súbežný odchod a útok), rýchlosť závisí od koncentrácií substrátu aj nukleofilu, preferuje primárne substráty a polárne aprotické rozpúšťadlá.
Okrem SN2 môže na rovnakom substráte konkurovať aj eliminácia E1 (najmä pri zvýšenej teplote alebo pri prítomnosti slabšieho nukleofilu/silnej bázy), preto sa často pozoruje zmes substitučných a eliminačných produktov.
Praktické príklady a experimentálne dôkazy
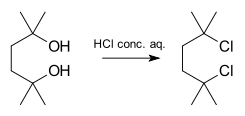
- Hydrolýza terciárnych alkylhalogenidov (napr. tert-butylchlorid vo vode) je klasický prípad SN1: pozoruje sa kinetika prvého rádu a vznik izopropylového (alebo iného) karbokationtu pred útokom vody.
- Dezaminácia terc-butylamónnych solí alebo dehydratácia terc-alkoholov v kyslom prostredí tiež postupuje cez karbokationt a sú často popisované ako SN1 (alebo súvisiace disociačné mechanizmy).
- Experimentálne dôkazy pre SN1 zahŕňajú: meranie rýchlostnej zákonitosti (prvý rád), vplyv rozpúšťadla na rýchlosť, pozorovanie racemizácie a detekciu/resonancia stabilizovaných karbokationtov v špeciálnych prípadoch.
Faktory ovplyvňujúce priebeh reakcie (zhrnutie)
- Substrát: terciárne a rezonancne stabilizované > sekundárne > primárne.
- Odchádzajúca skupina: čím lepší odchádzač, tým ľahšia SN1.
- Solvent: polar protické rozpúšťadlá podporujú SN1.
- Nukleofil: jeho sila má malý alebo žiadny vplyv na rýchlosť počiatočného kroku; slabé nukleofily sú akceptovateľné.
- Teplota: vyššia teplota môže zvýšiť konkurenciu E1.
SN1 je teda základný mechanizmus nukleofilnej substitúcie v organickej chémii, dôležitý pri porozumení reaktivity terciárnych systémov, pôsobenia rozpúšťadiel, stereochemických dôsledkov a možných preskupení, ktoré ovplyvňujú konečné produkty reakcie.