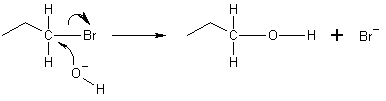
Nukleofil je druh, ktorý odovzdáva elektrónový pár elektrofilu a vytvára chemickú väzbu v reakcii. Všetky molekuly alebo ióny s voľným párom elektrónov môžu byť nukleofilmi. Tento pár elektrónov sa nazýva osamelý pár. Keďže nukleofily odovzdávajú elektróny, zodpovedajú definícii Lewisových báz.
Nukleofilný opisuje príťažlivosť nukleofilu k jadrám. Nukleofilita, niekedy označovaná ako sila nukleofilu, sa vzťahuje na nukleofilný charakter látky a často sa používa na porovnanie príťažlivosti atómov.
Neutrálne nukleofilné reakcie s rozpúšťadlami, ako sú alkoholy a voda, sa nazývajú "solvolýza". Nukleofily sa môžu zúčastňovať na nukleofilných substitučných reakciách. V týchto reakciách sa nukleofil priťahuje k úplnému alebo čiastočnému kladnému náboju.
Faktory ovplyvňujúce nukleofilitu
Nukleofilita závisí od niekoľkých hlavných faktorov:
- Nabíjanie: Negatívne nabité častice (anionty) sú zvyčajne silnejšie nukleofily ako ich neutrálny ekvivalent (napr. OH– vs H2O).
- Elektronegativita: Menej elektronegatívne atómy lepšie zdieľajú elektrónový pár a sú často silnejšími nukleofilmi (napr. I– vs F– v protických rozpúšťadlách).
- Polarizovateľnosť: Veľké, ľahko polarizovateľné anióny (ako I– alebo RS–) dobre reagujú pri tvorbe novo vznikajúcej väzby.
- Sterické prekážky: Priestorovo obmedzené nukleofily reagujú pomalšie; preto sú menšie a menej rozvetvené nukleofily efektívnejšie v SN2 reakciách.
- Rezónancia a delokalizácia náboja: Ak je náboj delokalizovaný (napr. karboxylátový anion), nukleofilita klesá, pretože voľný pár je menej dostupný.
- Solvent: V protických rozpúšťadlách (voda, alkohol) sú malé silno solvátované anióny ako F– výrazne oslabené. V aprotických polárnych rozpúšťadlách (DMF, DMSO) toto solvatovanie chýba a malé anióny sú relatívne silnejšie.
Rozdiel medzi nukleofilitou a zásaditosťou
Nukleofilita je kinetická veličina — popisuje, ako rýchlo nukleofil reaguje s elektrofilom. Zásaditosť (basicita) je termodynamická vlastnosť — vyjadruje rovnovážnu tendenciu akceptovať protón (H+). Aj keď sú často korelované (silné zásady bývajú aj silné nukleofily), existujú významné výnimky: napríklad I– je lepším nukleofilom než F– v protických rozpúšťadlách, ale I– je slabším zásadom ako F–.
Mechanizmy a typické reakcie
Nukleofily sa podieľajú na rôznych typoch reakcií:
- SN2 (bimolekulárna substitúcia): Priamoútočný mechanizmus, kde rýchlosť závisí od koncentrácie nukleofilu aj substrátu. Typické pre primárne a niektoré sekundárne alkylové halogenidy.
- SN1 (unimolekulárna substitúcia): Najprv sa tvorí karbokatión (pomocou odchodu skupiny), potom ho napadne nukleofil. Rýchlosť nezávisí priamo na nukleofile; typické pre tercierné substráty.
- Nukleofilná adícia: Nukleofily napadajú elektrofilné dvojné väzby, napr. karbonylové skupiny (príklady: adícia CN– k aldehydu alebo ketónu, hydridová adícia z NaBH4).
- Solvolýza: Špecifický prípad, keď je nukleofilom rozpúšťadlo (napr. voda alebo alkohol), čo vedie k vzniku substitučných alebo eliminačných produktov.
Bežné príklady nukleofilov
- Anióny: I–, Br–, Cl–, F–, OH–, RO–, RS–, CN–, N3–
- Neutrálne látky s voľným párom: H2O, ROH, NH3, RNH2, R2S
- Organické nukleofily: enoláty, organokovové činidlá (Grignardovy reagencie, organolitíkové zlúčeniny), karbanióny
Praktické ukážky
- SN2 príklad: OH– + CH3Br → CH3OH + Br– (rýchla priamej adduktívnej substitúcii pri makromolekulovej dostupnosti centrum útoku).
- SN1/solvolýza príklad: (CH3)3CCl + H2O → (CH3)3COH + H+ + Cl– (tvorba karbokatiónu, následná adícia vody ako nukleofilu).
- Nukleofilná adícia ku karbonylu: CN– + RCHO → RCH(OH)CN (tvorba kyanohydrínu).
Tipy pre kontrolu a navrhovanie reakcií
- Ak potrebujete rýchlu SN2 substitúciu, zvoľte silný, nenásobne substituovaný nukleofil a aprotický rozpúšťadlo (napr. DMSO).
- Ak sa chcete vyhnúť SN2 reakcii (napr. pri riziku eliminácie), zvážte použitie slabšieho nukleofilu alebo zmenu podmienok (nižšia teplota, iné rozpúšťadlo).
- Pri porovnávaní nukleofilov vždy uveďte kontext rozpúšťadla a sterické podmienky — poradie môže byť úplne odlišné v protickom vs aprotickom rozpúšťadle.
Celkové pochopenie nukleofilov a nukleofility pomáha pri predpovedaní a riadení organických reakcií — od jednoduchých substitúcií po zložitejšie syntetické postupy. Pri návrhu reakcií treba brať do úvahy kombináciu elektrónových vlastností, sterického profilu a prostredia (rozpúšťadlo, teplota, prítomnosť katalyzátorov).