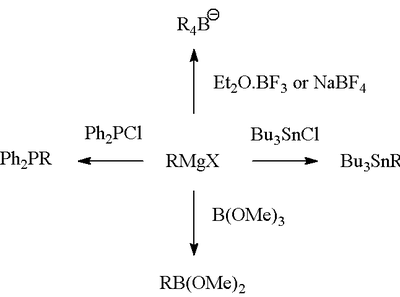
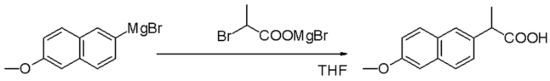
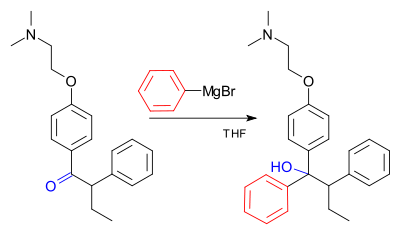
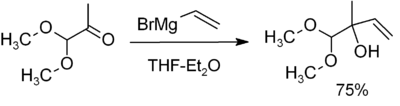Grignardova reakcia (vyslovuje sa /ɡriɲar/) je organokovová chemická reakcia, pri ktorej alkyl- alebo aryl-halogenidy reagujú s horčíkom za vzniku tzv. Grignardových činidiel (RMgX). Tieto látky pôsobia ako silné nukleofily a umožňujú nukleofilnú adíciu na elektrofilné atómy uhlíka v polárnych väzbách, napríklad v karbonylovej skupine. Typickým výsledkom je tvorba novej väzby uhlík–uhlík a zmena hybridizácie reakčného centra. Okrem C–C väzieb Grignardove činidlá umožňujú tvorbu väzieb uhlík–fosfor, uhlík–cín, uhlík–kremík, uhlík–bór a ďalších väzieb uhlík–heteroatóm.
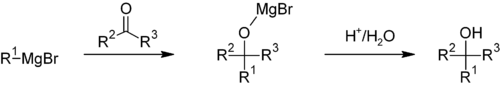
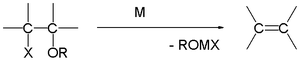
Mechanizmus
Vznik Grignardovho činidla prebieha pri reakcii organického halogenidu R–X s kovovým horčíkom (Mg) v suchom éteri alebo THF. Molekulárna povaha činidla nie je jednoduchý iónový pár, ale organokovový komplex alebo klaster viazaný na molekuly éteru. Existujú rôzne modely mechanizmu vzniku; iniciácia často zahŕňa single-electron transfer (SET) od Mg na R–X, tvorbu radikálov a následné zoskupenie do RMgX.
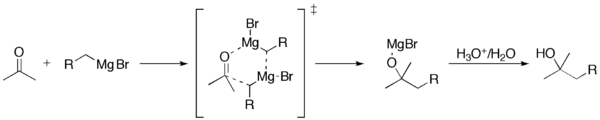
Pri typickej reakcii s karbonylom RMgX pôsobí ako nukleofil: atóm uhlíka viazaný na Mg napáda elektrofilný uhlík karbonylu, vzniká alkoxidový magnesiumsalt (MgX+ koordinovaný k alkoxidu). Po kyslom pracovnom kroku (napr. pridanie vody alebo NH4Cl) sa z tohto alkoxidu uvoľní príslušné alkoholné produkt. Schematicky:
- R–X + Mg → RMgX (v éteri alebo THF, tvorba komplexu)
- RMgX + R'–C(=O)–R'' → R–C(R')–O–MgX–R'' (alkoxidový komplex)
- pridanie H2O / H3O+ → R–C(R')–OH + MgX(OH)
Príprava a podmienky
Na prípravu Grignardových činidiel sa bežne používajú suché, aprotonické éterické rozpúšťadlá: diéter (éter dietylový) alebo THF. Tieto rozpúšťadlá koordinujú k horčíku a stabilizujú organomagnesium komplexy. Práca musí byť bez vody a kyslých protónov, preto sa používajú odpovedajúce pracovné postupy:
- vysušenie laboratórneho skla (flame-drying alebo sušenie v sušiarni),
- inertná atmosféra (dusík, argón),
- aktivácia povrchu horčíka (mechanické drvenie, pridanie jódovej pastilky, 1,2-dibrometánu, alebo ultrazvuk),
- pomalé pridávanie organického halogenidu za kontrolovanej teploty,
- monitorovanie iniciácie (exotermický štart, zmena farby roztoku).
Pre veľmi reaktívne alebo ťažko pripravené prípady sa používajú špeciálne formy horčíka (napr. Riekeho Mg) alebo katalytické metódy.
Rozpúšťadlá a agregácia
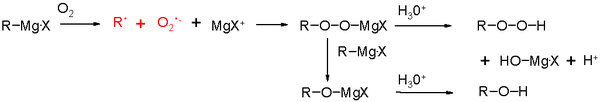
Grignardove činidlá sa v riešení vyskytujú ako komplexy s étermi a tvoria diméry alebo oligoméry. Preto sú vhodné len aprotické, koordinujúce rozpúšťadlá; protické rozpúšťadlá (voda, alkoholy, amíny) reagujú okamžite s RMgX a zničia činidlo. Atmosferická vlhkosť môže výrazne znížiť výťažok pri príprave RMgX, preto sa pri výrobe dbá na vylúčenie vody.
Typické reakcie a použitie
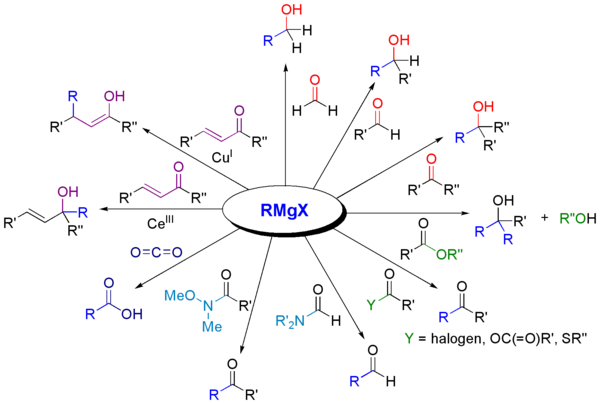
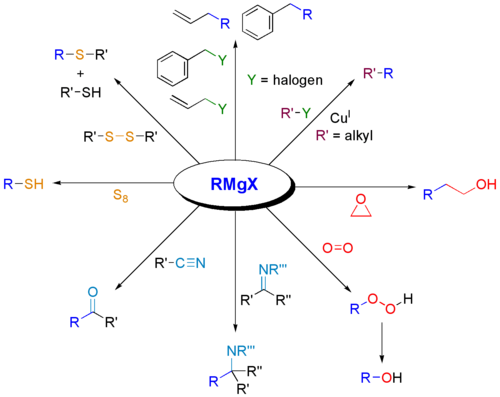
Grignardove činidlá sú základným nástrojom organickej syntézy pre konštrukciu C–C väzieb. Medzi najčastejšie použitia patria:
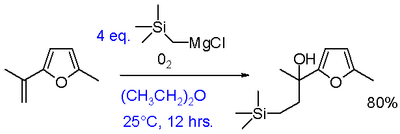
- Adícia na karbonyly – s formaldehydom, aldehydmi a ketónmi vedie k primárnym, sekundárnym alebo terciárnym alkoholom po kyslom pracovnom kroku.
- Reakcia s esterami a acid chloridmi – často vedie pri použití dvoch ekvivalentov RMgX k terciárnym alkoholom.
- Reakcia s oxiranmi (epoxidmi) – otváranie epoxidu prináša alkohol po protonačnom pracovnom kroku; útok prebieha na menej substituovanom uhlíku (zvyčajne).
- Karboxylácia CO2 – RMgX + CO2 → karboxylát (po pracovnom kroku karboxylová kyselina).
- Reakcia s nitrilmi – tvorba imínového komplexu, ktorý po hydrolyze dáva ketóny.
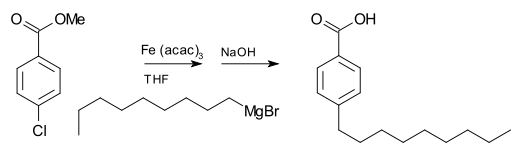
- Kumada cross‑coupling – v prítomnosti prechodného kovu (Ni, Pd) môžu byť Grignardove činidlá použité na spojenie s halogenidmi a vytvárať C–C väzby katalyticky (efektívna alternatíva k priamej SN2 s alkylhalogenidmi).
Obmedzenia a problémy
Grignardove činidlá majú niekoľko významných nevýhod a obmedzení:
- Citlivosť na vlhkosť a protické skupiny: reagujú s vodou, alkoholmi, fenolmi, amínmi, karboxylovými kyselinami a ďalšími protónovými zdrojmi a sú preto nekompatibilné s mnohými funkčnými skupinami.
- Problémy s tvorbou C–C via SN2: pri pokuse o priamu substitúciu alkylhalogenidom (R'–X) mechanizmom mechanizmomSN2 často dochádza k vedľajším reakciám (reduktívne dehalogenácie, Wurtzove typy spojenia, eliminácie) a efektívna priama SN2 C–C kondenzácia je obvykle nepraktická. Preto sa na priame spojenie dvoch alkylových komponentov častejšie používajú katalytické cross‑coupling reakcie (napr. Kumada).
- Reaktivita voči funkčným skupinám: nemôžu sa prímo kombinovať s látkami obsahujúcimi kyslé vodíky alebo silne elektrofilné halogenované skupiny bez chránenia funkčných skupín.
- Bezpečnosť: sú veľmi reaktívne, môžu byť pyrofórne pri kontakte so vzduchom a reagujú prudko s vodou, čo môže viesť k horľavým zmesiam a uvoľneniu plynných vedľajších produktov. Pracuje sa pod inertnou atmosférou a s vhodnými bezpečnostnými opatreniami.
Laboratórne tipy
- Pred prípravou skontrolujte a vysušte sklenené prístroje; použite inertnú atmosféru (N2/Ar).
- Ak iniciácia na horčíku neštartuje, pridajte malé množstvo jodidu, 1,2‑dibrometánu alebo použite mechanické premiešanie/ultrazvuk.
- Pri pridávaní substrátov udržiavajte kontrolu teploty – mnohé tvorby a následné adície sú exotermické.
- Pracovný postup (quench) uskutočnite pomaly a opatrne – pridávajte vodu alebo zriedenú kyselinu len postupne za miešania.
História
Grignardove reakcie objavil francúzsky chemik François Auguste Victor Grignard (univerzita v Nancy, Francúzsko). Za svoje práce o organomagnesium zlúčeninách a ich využití v syntéze dostal v roku 1912 Nobelovu cenu za chémiu.
Zhrnutie: Grignardova reakcia je kľúčová metóda v organickej syntéze na vytváranie nových C–C väzieb a ďalších C–X väzieb pomocou reaktívnych organomagnesium činidiel. Úspech reakcie závisí na suchých podmienkach, vhodnom rozpúšťadle, aktivovanom horčíku a kompetentnom pracovnom postupe kvôli vysokej reaktivite týchto činidiel.