Reakcia SN 2 (známa aj ako bimolekulárna nukleofilná substitúcia) je substitučná reakcia v organickej chémii. Ide o typ nukleofilnej substitúcie, pri ktorej osamelý pár nukleofilu atakuje elektrónovo deficitné, teda elektrónovo elektrofilné centrum a viaže sa naň. Tým je z molekuly vylúčená tzv. odchádzajúca skupina a prichádzajúca skupina ju v jednom kroku nahradí. Keďže sa v rýchlosťou určujúcom kroku reakcie zúčastňujú súčasne dva druhy (nukleofil a substrát), reakcia sa označuje ako bimolekulárna alebo SN2. Medzi anorganickými chemikmi je SN2 často známa aj ako výmenný mechanizmus.
Mechanizmus a prechodový stav
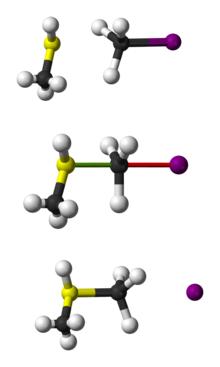
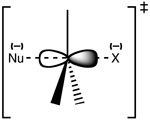
Mechanizmus SN2 je koncertovaný — väzba medzi nukleofilom a uhlíkovým centrom sa začína tvoriť súčasne s rozpadom väzby medzi uhlíkom a odchádzajúcou skupinou. Nukleofil zvyčajne realizuje tzv. backside attack, teda útočí proti strane, odkiaľ odchádzajúca skupina opúšťa centrálny atóm. V prechodovom stave vzniká pentakoordinačné rozdelenie nábojov, kde sú súčasne čiastočne vytvorené a čiastočne zlomené väzby — nie je stabilný medziprodukt, ale energetické maximum reakčnej cesty.
Kinetika
Rýchlosť reakcie SN2 je druhého rádu a opisuje ju zákon:
rýchlosť = k [substrát] [nukleofil]
To znamená, že rýchlosť závisí priamo od koncentrácií oboch zúčastnených zložiek. Aktivácia závisí aj od energie prechodového stavu — nižšia energia prechodového stavu → rýchlejšia reakcia.
Faktory ovplyvňujúce rýchlosť
- Typ substrátu: poradie reaktivity je všeobecne methyl > primárny > sekundárny; terciárne alkylové centrá sú stericky tak zablokované, že SN2 je veľmi pomalá alebo neprebieha.
- Nukleofil: silnejšie nukleofily (silnejší zásaditý alebo nabitý donor elektrónov) zvyčajne zrýchľujú SN2. Polarita a veľkosť nukleofilu tiež ovplyvňuje reaktivitu (menšie, menej solvatované anióny sú častejšie reaktívnejšie).
- Odchádzajúca skupina: lepšie odchádzajúce skupiny (stabilnejšie pri opustení ako ióny) podporujú SN2 — napr. I– > Br– > Cl– > F–.
- Rozpúšťadlo: polaritné aprotické rozpúšťadlá (napr. DMSO, acetónitril, DMF) zvyčajne urýchľujú SN2, pretože menej solvatizujú nukleofil a ten zostáva reaktívnejší. Protické rozpúšťadlá (napr. voda, alkohol) môžu nukleofil solvatovať a spomaľovať reakciu.
- Sterické prekážky: priestorové prekážky okolo elektrofilného centra bránia prístupu nukleofilov a výrazne spomaľujú reakciu.
- Elektronické efekty: susediace skupiny, ktoré stabilizujú prechodový stav alebo znižujú pozitívny charakter uhlíka, môžu ovplyvniť rýchlosť. Allylické a benzylické centrá sú často reaktívnejšie v SN2 pre delokalizáciu náboja.
Stereochémia
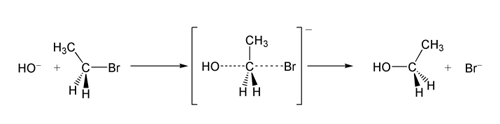
SN2 vedie typicky k Waldenovej inverzii konfigurácie pri stereocentrách — priame nahradenie prebieha s obrátením konfigurácie (analógie k "dverám, ktoré sa otvoria zozadu"). Preto sa SN2 používa na stereospecifické syntézy, ak je kontrola konfigurácie dôležitá. Výsledná racemizácia sa môže vyskytnúť len ak existujú ďalšie mechanizmy alebo keď sa reakcia vyskytuje cez viacero ciest.
Súťažné reakcie a praktické poznámky
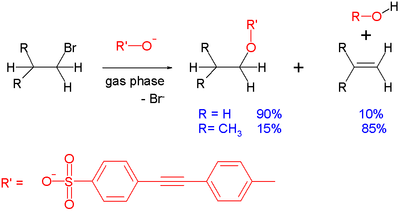
- Niekedy sú súčasne možné aj eliminácie (napr. E2), najmä pri silných zásadách a pri sekundárnych/terciárnych substrátoch. Podmienky (teplota, rozpúšťadlo, typ nukleofilu/zásady) určujú, ktorá cesta dominuje.
- SN2 býva preferovaná pri primárnych a methylových substrátoch a pri použití silných, nezosolvovaných nukleofilov v polar aprotických rozpúšťadlách.
- V praxi sa často používajú odchádzajúce skupiny ako halogenidy, sulfonáty (napr. tosylát) alebo iné, ktoré zlepšujú rýchlosť substitúcie.
Príklady
- Nukleofilná substitúcia halogenidov: CH3Br + OH– → CH3OH + Br– (typický jednoduchý príklad SN2 pri methylbromide).
- Prevod hydroxylu na lepšiu odchádzajúcu skupinu (napr. tvorba tosylátu) a následná nukleofilná substitúcia na zavedenie inej funkčnej skupiny.
Reakcia SN2 je preto kľúčovým mechanizmom v syntetickej organickej chémii, používaným pri konštrukcii väčšiny jednoduchých C–X alebo C–heteroatom väzieb pri zachovaní alebo kontrole stereo-centier. Znalosť faktorov, ktoré ovplyvňujú jej rýchlosť a stereochemické dôsledky, je základom plánovania chemických syntéz.