Sigmatropická reakcia v organickej chémii je pericyklická reakcia. Pri sigmatropickej reakcii sa nepoužíva katalyzátor a zahŕňa jedinú molekulu (nekatalyzovaný intramolekulárny proces). Mení jednu σ-väzbu na inú σ-väzbu. Názov sigmatropická je výsledkom spojenia dlho zaužívaného názvu "sigma" pre väzby typu jednoduchý uhlík - uhlík a gréckeho slova tropos, čo znamená obrat. Ide o reakciu preskupenia, čo znamená, že väzby v molekule sa posúvajú medzi atómami bez toho, aby z molekuly odišli nejaké atómy alebo do nej pribudli nové. Pri sigmatropickej reakcii sa substituent presúva z jednej časti systému s väzbami π do druhej časti v rámci vnútromolekulovej reakcie so súčasným preskupením systému π. Pravé sigmatropické reakcie zvyčajne nepotrebujú katalyzátor. Niektoré sigmatropické reakcie sú katalyzované Lewisovou kyselinou. Sigmatropické reakcie majú často katalyzátory z prechodných kovov, ktoré tvoria medziprodukty v analogických reakciách. Najznámejšie zo sigmatropických prestavieb sú [3,3] Copeova prestavba, Claisenova prestavba, Carrollova prestavba a Fischerova indolová syntéza.
Mechanizmus a charakteristika
Sigmatropické prestavby sú typicky koncertované pericyklické procesy: presun σ‑väzby sa deje súčasne so preskupením π‑systému cez cyklický prechodový stav bez izolovateľných iónových alebo radikálových medziproduktov. V prechodovom stave sa vytvárajú čiary prekrytia medzi orbitálmi, ktoré umožňujú plynulé presunutie väzby. Migrácia môže zahŕňať vodík (napr. [1,5]-H prestavba) alebo skupiny uhlíka (napr. [3,3] Cope alebo Claisen).
Klasifikácia: [i,j] označenie, suprafaciálne vs. antarafaciálne
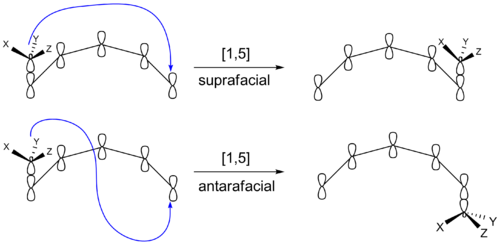
Sigmatropické prestavby sa označujú ako [i,j], kde i a j sú počty atómov π‑systému na oboch stranách migrujúcej σ‑väzby. Dôležité je, či sa migrácia uskutočňuje suprafaciálne (na tej istej strane π‑systému) alebo antarafaciálne (na opačných stranách). Suprafaciálne posuny sú geometricky ľahšie dosiahnuteľné a preto častejšie; antarafaciálne posuny sú často zakázané z priestorových dôvodov v lineárnych alebo cyklických systémoch a vyskytujú sa zriedka.
Pravidlá orbitalnej symetrie
Priebeh a povolenie sigmatropickej reakcie ovplyvňujú pravidlá zachovania orbitalnej symetrie (Woodward–Hoffmann). Pod týmto uhlom pohľadu sú niektoré [i,j] prestavby termicky povolené ako koncertované suprafaciálne procesy (napríklad mnoho [3,3] prestavieb a [1,5]-H presunov), zatiaľ čo iné sú termicky zakázané a vyžadujú fotochemickú aktiváciu alebo prebiehajú cez alternatívny (napr. stepwise) mechanizmus. Tieto pravidlá určujú, ako sa symetria frontierových orbitalov (HOMO/LUMO) môže zachovať počas cyklického prechodu.
Typické príklady a syntetické použitie
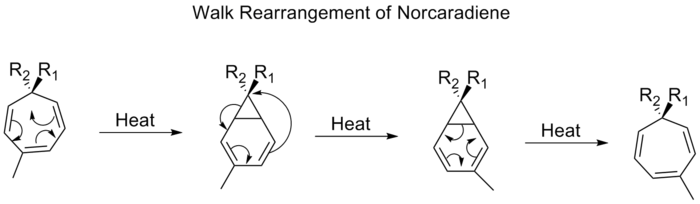
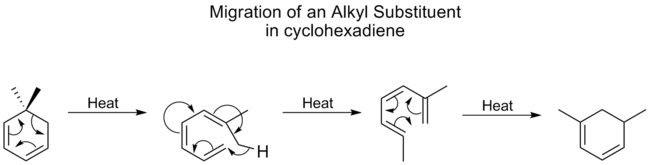
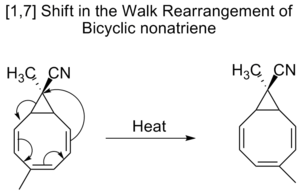
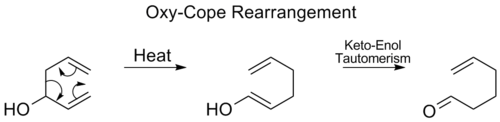
- Copeova prestavba ([3,3]) – prestavba 1,5‑dienov cez šesťčlenný cyklický prechodový stav. Reakcia je často reverzibilná a jej termodynamický smer závisí od substitučných efektov a uvoľnenia napätia (napr. aromatizácia ako hnacia sila).
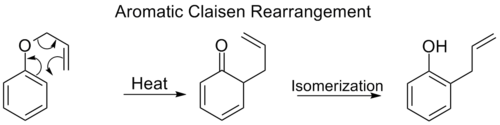
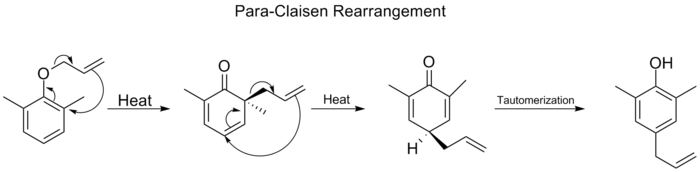
- Claisenova prestavba ([3,3]) – pri klasickej Claisenovej prestavbe sa allyl(vinyl/aryl)éter prestaví na γ,δ‑n-nenasýtený karbonyl alebo na ortho‑allylované fenoly (v prípade allylfenyléterov). Lewisove kyseliny alebo teplo často urýchľujú tento proces.
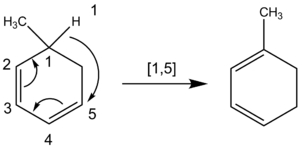
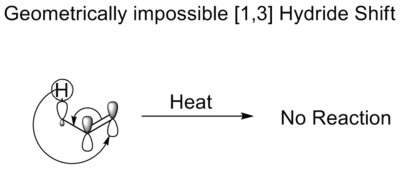
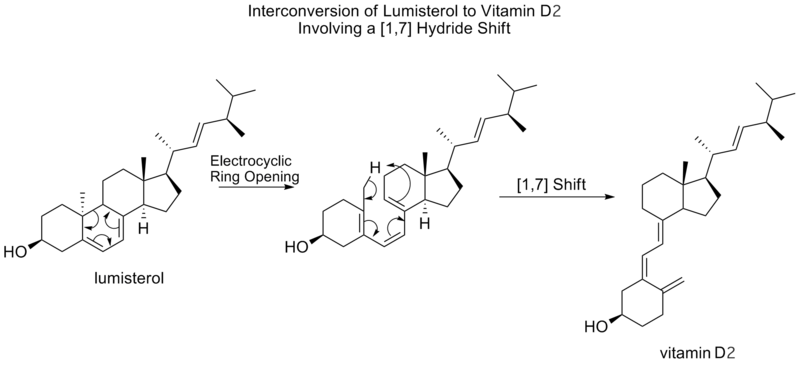
- [1,5]-hydridové presuny – bežné pri konjugovaných dienoch, vodíkový atóm sa presúva na vzdialenosť piatich atómov v rámci concertovaného cyklického prechodu.
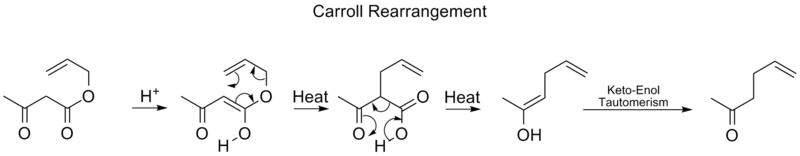
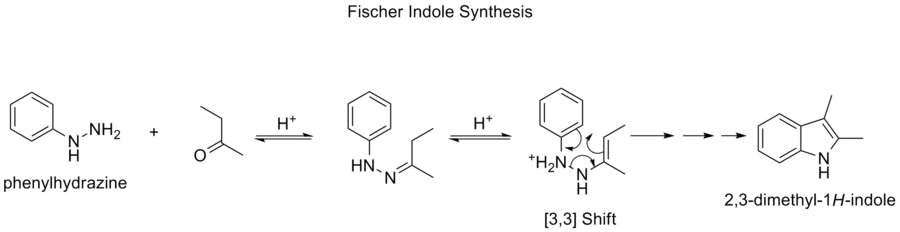
- Carrollova prestavba, Fischerova indolová syntéza – zložitejšie prestavby využívané pri syntéze heterocyklických jadier a pri tvorbe C–C väzieb v prírodných produktoch a liečivách.
Stereochémia, kinetika a katalýza
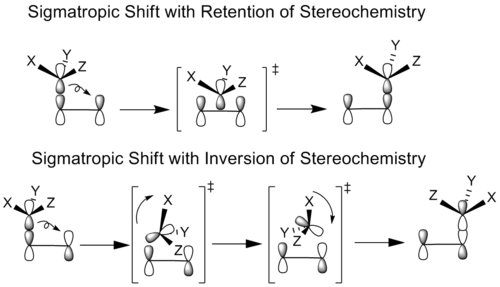
Stereochemické výsledky závisia od typu migrácie (suprafaciálne zvyčajne vedie k zachovaniu určitej stereochemie). Energetické bariéry sigmatropických prestavieb sú často stredné až vysoké, preto sa častokrát vyžaduje zvýšená teplota. Katalýza Lewisovými kyselinami môže znížiť aktivačnú energiu (napr. koordinácia ku kyslíku v Claisenovej prestavbe), zatiaľ čo prechodné kovy môžu otvoriť alternatívne, často stepwise, reakčné cesty, ktoré sa dajú využiť na riadenie reaktivity a selektivity.
Praktické poznámky
Pri plánovaní syntéz využívajúcich sigmatropické prestavby je potrebné zvážiť:
- geometriu substrátu (ktorá určuje, či je suprafaciálna/antarafaciálna cesta dostupná),
- energetickú bilanciu medzi východiskovým a produktovým stavom (napr. úľava napätia alebo aromatizácia môže poháňať rovnováhu),
- možnosť konkurencie so stepwise mechanizmami pri prítomnosti stabilných karbokatiónových alebo radikálových centier,
- využitie katalyzátorov alebo fotochemickej aktivácie pri termicky zakázaných prestavbách.
Sigmatropické reakcie sú mocným nástrojom v organickej syntéze na selektívne presuny skupín a tvorbu nových C–C alebo C–X väzieb bez pridaných reaktantov, pričom ich použitie vyžaduje pochopenie orbitálnej symetrie, geometrie a termodynamiky systému.

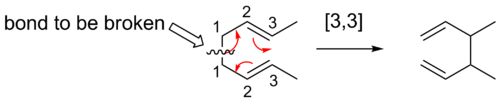
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)